대장균군(Coliform group)과 대장균(Escherichia coli)
대장균군이란 35~37℃에서 배양 시 lactose를 분해하여 산과 가스를 생성하는 그람 음성균으로 호기성 또는 통성혐기성 간균을 총칭한다. 여기에는 Citrobacter, Enterobacter, Escherichia, Hafnia, Klebsiella, Serratia 속 등이 포함된다. 그러나 대장균군과 같은 성질을 가진 세균은 자연계에 널리 분포하고 있기 때문에 설령 측정한 식품으로부터 대장균군이 검출되었다 하더라도 반드시 분변에 오염되었다고 판단하기에는 무리가 있다.
따라서 사람과 온혈동물의 분변에 반드시 존재하는 Escherichia coli 존재여부를 측정함으로서 정확한 분변의 오염여부를 판단할 수 있다. Escherichia coli(EC) 배지에서 45.5±0.5℃(Air incubator) 또는 44.5±0.2℃(Water bath)에서 24시간 배양하였을 때 산과 가스를 생성하며, indole, methyl red 양성반응, voges-proskauer, citrate를 이용하지 못하는 균을 Escherichia coli(대장균) 이라 한다.
따라서 사람과 온혈동물의 분변에 반드시 존재하는 Escherichia coli 존재여부를 측정함으로서 정확한 분변의 오염여부를 판단할 수 있다. Escherichia coli(EC) 배지에서 45.5±0.5℃(Air incubator) 또는 44.5±0.2℃(Water bath)에서 24시간 배양하였을 때 산과 가스를 생성하며, indole, methyl red 양성반응, voges-proskauer, citrate를 이용하지 못하는 균을 Escherichia coli(대장균) 이라 한다.
장구균(Enterococcus spp.)
대장균의 분포가 분변에 의한 오염과 반드시 일치하지 않는 경우가 있는 것과는 달리 장구균는 사람과 온혈동물의 분변에 항상 존재하고 인축의 분변으로 오염되지 않은 환경에서는 검출되지 않으므로 위생지표세균으로 이용된다. 장구균은 그람양성 구균으로 catalase 음성, glucose, maltose를 분해하여 산을 생성하고 lactose, sucrose도 대부분의 장구균은 분해한다.
영양요구성이 복잡하여 단순한 당류와 염류가 포함된 배지에서는 발육하지 않고 여러가지 vitamin, amino acid, 유기화합물을 필요로 한다. 장구균은 대장균군에 비해 외계에서 증식이 어렵고, 자연계(물, 토양)에는 비교적 적게 존재하며, 냉동했을 때에는 사멸률이 대장균군보다 낮기 때문에 냉동식품의 오염지표 세균으로 적합하다. 장구균은 AC배지, KF한천배지 등을 사용하여 35~37℃에서 48시간 배양하여 검출한다.
영양요구성이 복잡하여 단순한 당류와 염류가 포함된 배지에서는 발육하지 않고 여러가지 vitamin, amino acid, 유기화합물을 필요로 한다. 장구균은 대장균군에 비해 외계에서 증식이 어렵고, 자연계(물, 토양)에는 비교적 적게 존재하며, 냉동했을 때에는 사멸률이 대장균군보다 낮기 때문에 냉동식품의 오염지표 세균으로 적합하다. 장구균은 AC배지, KF한천배지 등을 사용하여 35~37℃에서 48시간 배양하여 검출한다.
비브리오 파라헤몰리티쿠스 (Vibrio parahaemolyticus, 장염비브리오균)
V. parahaemolyticus는 1950년 10월 일본 오사카 남부에서 멸치포(Engraulis japonica)를 먹고 식중독 증상을 보인 272명의 환자 중 20명이 사망한 사건을 계기로 처음 알려지게 되었다. 이 균은 해수 및 각종 해산물에 서식하는 저도 호염성균으로 수산물을 즐겨 먹는 한국, 일본을 비롯한 동남아시아 각국에서 여름철에 빈번하게 발생하는 세균성 식중독 원인균의 하나로 잘 알려져 있다.
특징
그람음성, 통성혐기성 간균으로 액체에서는 극단모성편모만을 갖지만 고체에서는 극단모성편모와 주모성편모를 함께 형성한다. 이 균은 식염농도 0.5~10%에서 증식하지만 3% 전후가 최적 식염농도이다. 생육 최적온도는 30~37℃이며, 최적 pH는 7.5~8.5이다. 특히 산성 조건에서는 증식이 나쁘며, pH 4.5 이하에서는 급속하게 사멸한다. 저온 및 고온에도 약해 10℃ 이하, 45℃ 이상에서는 거의 생육하지 못하며 60℃에서 10분간 가열에 의해 사멸한다. 또한 염분이 없는 수돗물에서는 쉽게 사멸하는 특징이 있다.
하지만 다른 세균에 비해 증식속도가 빨라 최적조건에서는 약 10분에 1회 분열하기 때문에 온도가 높은 여름철에는 특히 주의할 필요가 있다. 이 균은 주로 해수역 또는 기수역에 서식하는데 수온이 17℃ 이상으로 상승하면 해수에서의 검출률은 상승한다. 이 균의 H항원은 모든 균에서 공통이기 때문에 13종류의 O항원과 75종류의 K항원으로 분류되며 기본적으로 O 및 K항원의 조합 으로 분류된다. 장염비브리오(V. parahaemolyticus)의 주요한 병원성 인자는 내열성 용혈독(thermostable direct hemolysin, TDH) 과 내열성 용혈독 관련용혈독(TDH related hemolysin, TRH) 등이 있다.
하지만 다른 세균에 비해 증식속도가 빨라 최적조건에서는 약 10분에 1회 분열하기 때문에 온도가 높은 여름철에는 특히 주의할 필요가 있다. 이 균은 주로 해수역 또는 기수역에 서식하는데 수온이 17℃ 이상으로 상승하면 해수에서의 검출률은 상승한다. 이 균의 H항원은 모든 균에서 공통이기 때문에 13종류의 O항원과 75종류의 K항원으로 분류되며 기본적으로 O 및 K항원의 조합 으로 분류된다. 장염비브리오(V. parahaemolyticus)의 주요한 병원성 인자는 내열성 용혈독(thermostable direct hemolysin, TDH) 과 내열성 용혈독 관련용혈독(TDH related hemolysin, TRH) 등이 있다.
-
내열성 용혈독(TDH)
장염비브리오(V. parahaemolyticus)에는 적혈구 막에 구멍을 내어 용혈하는 균과 용혈하지 못하는 균이 존재하는데 용혈현상(Kanagawa phenomenon, KP)의 원 인물질은 TDH 이다. 식중독 환자로부터 분리된 장염비브리오(V.parahaemolyticus)의 대부분은 TDH 양성이지만(TDH 양성균), 어패류 및 해수 등 의 환경에서 분리한 대부분의 균은 TDH를 생산하지 않은 균주(TDH 음성균)이다. TDH는 165개의 아미노산으로 구성된 이량체 단백질로 분자량은 약 42 kDa 의 산성 단순단백질이다. 열에는 강해 100℃에서 10분 가열에 의해 실활되지 않은 내열성 독소이다. 용혈작용 외에 세포독성, 세포독성, 심장독성 및 장관독성 등을 나타낸다. -
내열성 용혈독 관련용혈독(TRH)
1988년 인도양의 몰디브 여행자의 설사 가검물로부터 KP 음성이지만 용혈능 등을 나타내는 병원성 장염비브리오(V. parahaemolyticus)에서 TDH와 아미노산 수준으로 67%의 상동성을 나타내는 용혈독소가 발견되었는데 이 독소를 TRH라부른다. TRH 또한 165개의 아미노산으로 구성된 단백질로 용혈능, 세포독성, 심 장독성 및 장관독성 등의 활성을 나타낸다. 열에는 약해 60℃에서 10분 가열에 의해 실활되는 이열성 독소이다.
원인식품과 오염경로
장염비브리오(V. parahaemolyticus)에 의한 식중독 사고는 기온이 상승하는 5~10월에 주로 발생한다. 원인식품은 생식의 어패류이며 그 외에 초밥의 생 선이 원인이 되는 경우도 있으며 생선에 부착하고 있는 균이 칼이나 도마 등의 조리 기구를 통해 다른 식품을 오염시켜 식중독을 일으키는 경우도 있다. 이 균에 의한 식중독은 한국, 일본과 동남아시아에서 발생빈도가 높고, 공항에서 검사한 설사환자의 검역에서도 살모넬라 등과 같이 빈번하게 분리되고 있다. 우리나라의 장염비브리오(V. parahaemolyticus)에 의한 식중독 통계를 보면 2002년부터 2008년까지 7년간 146건 발생에 3,393명의 환자가 발생하여 매년 전체 세균성 식중독 발생건수의 약 20%를 차지하며, 병원성대장균, 살모넬라에 이어 3위로 많이 발생하였다. 일본 후생성의 1996년 식 중독 통계에 의하면 장염비브리오(V. parahaemolyticus)는 세균성 식중독 발생사례에서는 2위로 27.9%를 차지하였으며 환자수 5,241명이 보고되었으나 사망자는 없었다. 한편, 동남아시아나 인도에서도 장염비브리오(V.parahaemolyticus)에 의한 위장염 환자는 상당히 많으나 이들 지역에서는 어 패류의 생식이 직접적인 원인이 아니고, 비위생적인 환경에 의한 조리식품의 2차 오염 및 음료수의 오염이 주된 원인이라고 생각되어진다. 어패류를 생식하지 않은 미국, 오스트레일리아, 아프리카, 동유럽에서도 장염비브리오(V. parahaemolyticus)에 의한 식중독 사고사례는 보고되고 있다.임상증상 및 치료
잠복기는 보통 6~18시간이지만 2~3시간에 발병하는 예도 있다. 증상은 심한 복통, 설사, 발열, 구역질, 구토 등의 전형적인 급성위장염 증상을 나 타낸다. 거의 열이 없는 상태로 경과하는 예도 있으며 보통 2~3일 또는 수일이 지나면 회복된다. 설사는 일반적으로 수양성(水樣性) 변이지만 이질과 같이 출혈성 설사를 하는 경우도 있다. 일반적으로 사망자가 나오는 일은 거의 없으나 노약자는 탈수에 의한 심쇠약사를 일으키는 경우도 있다. 우 리나라에서는 장관 외 감염사례는 드물지만 유럽과 미국에서는 상당히 많은 예가 보고되어 있다. 이들 사례에는 중이염, 발의 창상 및 패혈증 등이 있으며, 패혈증 환자는 모두 간경변 등의 기초질환이 있는 경우였으며 결과적으로는 이 감염에 의해 사망하는 예도 있다. 그러나 이들 경우의 대부 분은 경구감염보다는 해수욕 시 피부 외상에 오염된 해수로부터 감염되는 것으로 생각된다. 치료는 위장염에 new-quinolon계 등의 항생물질 투여가 행하여지며 탈수에는 수액보충이 필요하다. 장염비브리오(V. parahaemolyticus)는 chloramphenicol, oxytetracycline 및 ciprofloxacin 등의 항생제에는 감수성이나 ampicillin, streptomycin, kanam-ycin 및 cefazolin 등에는 저항성을 가지는 균주가 많으며, 특히 양식어류에 서는 다재항생제 내성균의 출현이 증가하고 있는 추세라 주의가 요망된다.예방법
예방법은 다른 세균성 식중독의 경우와 유사하나 이 균은 생어패류의 섭취가 주된 감염경로이기 때문에 6~10월의 여름철에는 어패류의 생식에 주 의할 필요가 있다.- 01장염비브리오(V. parahaemolyticus)는 60℃에서 10분 가열에 사멸하기 때문에 가열 조리하면 식중독은 예방할 수 있다.
- 02저온에는 약해 0~2℃에서는 어패류에 부착되어 있는 균은 24~48 시간에 사멸하기 때문에 어패류는 4℃ 이하에서 보존한다.
- 03담수에 약하기 때 문에 어패류를 담수에서 잘 씻으면 표면에 부착되어 있는 균은 사멸한다.
- 04식초 등에 약하기 때문에 산을 사용해도 균을 사멸시킬 수 있다.
- 05발병에는 다량의 균(108cells)이 필요하기 때문에 저온보관, 가열조리후 바로 먹거나 2차 오염을 방지하는 등의 원칙적인 예방법을 준수하는 것 이 중요하다.
비브리오 불니피쿠스(Vibrio vulnificus, 비브리오 패혈증균)
V. vulnificus는 1970년 미국의 New England 해안에서 피부상처로 침입하여 괴저병을 유발하는 원인균으로 ‘Roland’에 의해 처음으로 보고되었다. 그 후 ‘Zide’ 등은 사지에 다형성 홍반을 수반하고 사망한 패혈증의 예를 보고하였으며 미국 질병관리센터(Centers for Disease Control and Prevention, CDC)는 분리균주를 상세하게 검토한 결과, 창상 및 혈액 중에서 분리한 균주는 명확하게 장염비브리오와는 다르고 특히 lactose를 천천히 분해한다는 점 등 생화학적으로 구별되어지는 점으로 ‘Hollis’ 등은 lactose-fermenting vibrio(또는 L+vibrio)라고 칭하였다. 한편 같은 시기 ‘Reichelt’ 등은 이 균이 사람에게 창상(wound=vulnus)을 만드는 점에서 Beneckea vulnificus라고 명명하였다. 그 후 이 균에 대한 다양한 논의가 있었지만 ‘Farmer’는 이를 통일하여 1979년에 Vibrio vulnificus라고 명명하였고 1980년에 승인되었다. 따라서 비브리오 패혈증은 비브리오속 중에서도 비교적 신종에 속한다.
특징
V. vulnificus는 그람음성의 만곡형 간균이며 극단모성 편모를 가지는 저도호염성의 해양세균이다. Sucrose, haptanose, L-serine, putresine은 이용하지 못하나 D-galactose, cellulose, D-gluconate, L-tyrosine은 이용한다. 8% 이상의 식염농도에서 증식하지 못하며, 40℃에서 생육이 가능하며 arginine dehydrogenase와 acetoin 생산능이 있다. V. vulnificus는 lactose의 분해성에서 V. parahaemolyticus와 다르며, colistin에는 내성이지만 ampicillin과 carbenicillin에는 감수성이어서 다른 유사한 세균과 구별된다.
생태 및 성상
V. vulnificus 는 굴, 대합 및 피조개 등의 패류와 생선, 저질과 플랑크톤에서도 분리되며, 수온이 20℃ 이상이며 염분이 낮은 해역에서 빈번히 검출된다고 알려져 있다. 일본에서 분리된 V. vulnificus를 O항원에 의해 15개 혈청형으로 구분하며 혈청형 O1과 O4가 환자에서 빈번히 분리된다. 우리나라의 경우도 환자나 어패류에서 분리된 V. vulnificus의 혈청형은 O4형이 자연계 분리균주의 49%, 환자분리 균주의 64%를 차지하며, O1형은 각각 21%와 13%로 나타나 일본과 비슷한 경향을 나타내었다. 자연계 분포와 혈청형의 빈도, 환자에서 분리된 혈청형의 빈도가 비슷한 것은 이 세균의 병원성은 어느 혈청형이나 비슷하다는 가정을 할 수 있을 것으로 생각되어진다.비브리오 패혈증 균이 서식하기 좋은 조건
- 01하천이 바다에 유입되는 지역으로 염분이 낮고 유기물질의 오염이 많은 기수지역의 물이다.
- 02주로 항내나 인구가 밀접한 도시주변의 바닷물에서 검출되나 동일한 시기에 먼 바닷물에서는 검출되지 않는 것으로 볼 때 주로 연안에서 서식하고 있다.
- 03뻘 또는 모래가 많이 있고 수심이 낮아서 외기의 영향을 많이 받는 지역에서 기온이 높을 때이다.
역학
우리나라에서는 1979년 처음으로 패혈증 환자가 발생하였으나 정확한 원인을 알지 못하였고, 1981년에 그 원인균이 V. vulnificus인 것으로 밝혀지게 되었다. 1980, 1981, 1983년에 환자가 발생한 것으로 보고되었고 그 중 12명이 사망함으로써 사회적인 문제로 발전하게 되었다. 이러한 과정에서 이 병을 괴저병 또는 패혈증이라고 하였으며 이는 임상증상이 피부가 불에 덴 것 같은 겉모양을 띤다(vulnifucs=wound)는 의미에서 유래하였다. 우리나라에서는 1985년 7월에 이 균에 의한 질병을 비브리오 패혈증으로 정식 명명되었으며, 2000년 8월에는 법정전염병 제3군으로 지정되어 있다.국내에서 이 균에 의한 패혈증 환자는 주로 여름철인 6~9월경에 나타나고 있으나 1988년에는 3월경, 1992년과 1993년에는 5월경에 첫 감염자가 발생되고 있는 것으로 조사되었다. 특히 전남지방에서 비브리오 패혈증 환자가 많이 발생하는데 그 이유로는 전남지역이 위치상 다른 지역보다 남쪽에 위치하고 있어 수온이 높고 지정학적으로 갯벌에 많아 이 균이 서식하기가 용이하며 타 지역에 비해 2면이 해안으로 둘러싸여 있고 섬들이 많으며 해안가에 상주하는 인구가 많기 때문이라고 생각된다. 2001년부터 2008년까지 8년간 국내에서 발생한 V. vulnificus 환자 발생 수 및 사망자수를 보면 총 491명의 환자가 발생하여 243명이 사망하였으며 사망률은 약 49.5%였다. 수산물을 생식하는 일본과 비교하여 이 균에 의한 환자 발생 수 및 사망자수가 많은 것은 수산물을 위생적으로 다루지않는 점과 음식점이 아닌 비공식적인 루트로 수산물을 생식하기 때문인 것으로 여겨진다.
병원성인자
비브리오 패혈증의 병원성 인자는 표 2-3에 나타내었다. 균체외부 요인으로는 협막의 존재를 들 수 있다. 병원성이 강한 균 중에서는 혈청의 살균작용에 대해서 저항성을 나타내는 것이 있고, 이들 물질이 다당체로 된 협막의 존재와 상관성을 나타내는 것이 전자현미경 관찰 및 면역화학적 연구에 의해 증명되었다.
표 2-3. Vibrio vulnificus가 생산하는 독성요인과 작용기작
| 독성요인 | 독 작 용 |
|---|---|
| Capsule | Antiphagocytic effect |
| LPS (lipopolysaccharide) |
Pyrogen, Endotoxin shock |
| Hemolysin | Cytolysis, Vascular permeability enhancing action, Lethal activity in mice |
| Protease | Proteolysis, Activation of kinin system, Degradation of mast cell(Vascular permeability enhancing action) |
| Phospholipase A2 | Hydrolysis of phospholipids |
| Siderophore | Iron-chelator ; Stimulation of bacterial growth |
기질로서는 콜라겐, 엘라스틴, 카제인 등을 분해하는 것으로 균체의 침입성에 있어서도 이 인자가 관여하고 있을 가능성은 크다. 또 강한 피부 모세혈관 투과성 항진활성을 가지고 있으며 rat의 비만세포에서 histamine을 유리시키고 모르모트에서는 plasmakinin의 생성을 촉진하는 것으로 알려져 있다. 이와 같이 효소는 염증의 메디에타로 작용하고, 이 인자가 감염증의 주 증상인 국부의 조직 장해 등에 관여한다고 예상할 수 있다. 최근 이 균의 protease는 hemoglobin과 myoglobin등의 heme 함유 단백질에서 heme을 유리시키고 이 균의 생육에 필요한 철원을 공급하는 역할을 한다는 것을 in-vitro 계에서 확인하였다. 수중에는 1cm당 철 원자는 1,000개 정도 밖에 존재하지 않고 그 대부분의 철 이온은 3가로 산화된 상태로 존재하고 있다. 균체는 3가의 철을 이용할 수 없기 때문에 이온과 특이적으로 킬레트해 균체 내에 철원을 공급하는 sideropore는 이 균의 생존 및 증식에 공헌하고 있다고 생각되어진다. 또 균체가 생체 내에 침입하여 감염을 일으킨 경우는 숙주측은 transferrin등의 철 결합 단백질을 분비하여 혈청철의 저하를 일으키고, 병원체의 생존을 곤란하게 하는 nutritional immunity를 일으키지만, 이와 같은 경우에도 이 인자는 효율적으로 철을 흡수여 균의 생존을 조정하고 있다고 생각되어진다.
1981년 ‘Kreger’과 ‘Lockwood’는 V. vulnificus가 배양액에 적혈구와 CHO세포를 녹이는 cytolysin(세포용해 독소)를 분비하는 것을 보고하였다. 이 독소는 분자량 56,000 Da의 소수성 단백질로 막의 콜레스테롤과 결합한 후 막상에서 수 분자가 중합하고 직경 3mm 전후의 구멍을 뚫어 세포의 파괴를 일으킨다. 이 cytolysin은 적혈구, 각종의 배양세포만이 아닌 콜레스테롤과 인지질로 구성되어진 인공막인 리포솜도 파괴할 수 있다. Cytolysin은 471개의 아미노산으로 구성되어 있으며, 그 분자량은 53,039 Da이다. 이 유전자(vvhA)의 46bp 상류에는 549bp의 별도의 ORF(vvhB)가 존재한다. vvB가 vvA에 상당히 근접하고 있다는 점, vvhB에 대한 명확한 프로모타가 발견되지 않은 점, vvhB를 결실하면 cytolysin의 생산되지 않는다는 점으로 보아 cytolysin 생산 시 필요한 유전자이고 vvhA와 오페론을 형성하고 있을 가능성이 있는 것으로 생각되어진다. vvhA 유전자는 V. vulnificus에 특유의 유전자이기 때문에 V. vulnificus를 검출에 유용하게 이용되어지고 있다.
임상증상 및 치료
비브리오 패혈증의 감염경로는 크게 두 가지로 구별된다. 하나는 어패류의 생식에 의해 발병하는 경구감염이고 다른 하나는 상처부위가 해수에 접촉함으로서 균이 침입해서 발병하는 창상감염이다. 경구감염의 증상은 급작스런 발열, 오한, 정신쇠약감 등으로 시작하여 때로는 구토와 설사도 동반한다. 잠복기는 16~24시간이며 발병 30시간 전후에 대부분의 환자에서 피부병소가 사지, 특히 하지에서 부종, 발적, 반상출혈, 수포형성, 궤양, 괴사 등의 모습으로 나타난다. 사망률은 약 70% 전후로 매우 높다. 창상감염의 경우에는 창상으로 해수에 있던 균이 침입하여 창상부위에 부종과 홍반이 발생하며 증상은 급격히 진행되어 대부분의 경우 수포성 괴사가 생긴다. 잠복기는 12시간이며 대부분 기초질환이 없는 청장년층은 항생제 및 외과치료에 의해 회복되지만 노인이나 기초질환자는 사망률이 약 30% 전후이다. 우리나라와 일본에서는 경구감염이 압도적으로 많으나 미국의 경우에는 창상감염이 약 50% 정도를 차지한다. 이는 우리나라와 일본의 경우는 어패류를 생식하는 식습관에 기인하는 결과라 사료된다. 비브리오 패혈증 감염자의 특징은 만성간질환자(간염, 간경변, 간암), 당뇨병환자, 습관적 음주 자, 철 결핍성 빈혈로 철분제를 복용하고 있는 자, 면역기능이 저하되어 있는 자, 스테로이드제 복용자 등에 집중되어 있으며, 기초질환이 없는 건강한 사람이나 젊은 사람의 경우 감염예가 드물며, 감염되어도 가벼운 설사나 복통수준에서 끝나며 중증으로 발전하는 경우는 거의 없다. 치료법은 조기에 적절한 항생제를 투여하면 거의 100% 치료할 수 있다. 치료약제로서는 tetramycine이 잘 알려져 있으며, 그 외 chloramphenic -ol, gentamycin, cephalothin, tobramycin, nalidxic acid, ampicillin등의 항생제가 이용되고 있다. 그러나 균주의 증식속도가 매우 빠르기 때문에 패혈증까지 증상이 진행하면 치료가 늦어져서 대부분이 사망하기 때문에 패혈증이 의심되는 경우에는 신속히 가까운 병원을 방문하여 적절한 치료를 받는 것이 무엇보다 중요하다.예방법
비브리오 패혈증은 갯벌이 있고 하천수가 바다로 유입되어 유기물질의 오염도가 높아지고 염분이 낮은 특수지역에서 수온이 높은 여름철에 주로 문제가 되므로 이런 지역에서 생산된 수산물(특히 생식용 패류)에 대한 특별한 관리가 요구된다. 그리고 여름철에 이런 지역의 주민들 중 건강이 나쁜 사람들(간질환, 당뇨병 등의 소모성 질환자 및 알코올 중독자)을 대상으로 주의를 환기시킬 필요가 있다. 건강한 사람이 감염된 경우는 극히 드물기 때문에 모든 사람을 대상으로 생선회의 섭취를 금지시킬 필요는 없다고 본다.- 01건강에 문제가 있는 사람은 여름철에 어패류의 생식을 가급적 피하고 가열된 어패류를 섭취할 것
- 02어획에서 소비에 이르기까지 전 과정을 철저히 저온 저장하여 균의 증식을 최대한 억제한다.
- 03하절기에는 가능한 어패류의 생식을 삼간다(특히 만성질환자 등의 취약자).
- 04만약 생식할 경우 어패류를 담수에 일정시간 담가 두었다가 깨끗이 씻는다.
- 05활어패류를 취급하는 업소에서는 오염된 해수의 사용을 삼가고 소독수와 담수 등을 사용하여 주방을 철저히 소독한다.
- 06피부에 상처가 있는 사람은 어패류 취급을 삼가며, 어패류 취급 시 상처를 입지 않도록 주의한다.
비브리오 콜레라(Vibrio cholerae)
V. cholerae의 혈청형이 O1/O139 이외의 콜레라를 non-agglutinable(NAG) 비브리오 또는 non-cholerae vibrio(NCV)로 부르며, 현재에는 혈청형 O1 이외의 균을 V. cholerae non-O1/O139로 총칭한다.
특징
V. cholerae non-O1은 통성혐기성, oxidase 양성, 포도당 발효성의 그람음성 간균이다. 콜레라와 같이 약간 만곡한 콤마상의 형태를 하고 있고 1개의 편모(극단모성 편모)로 운동한다. V. cholerae non-O1/O139는 식염이 없는 무염 펩톤수에서 발육할 수 있으나 식염이 존재하면 발육이 촉진되기 때문에 연안해역과 하구 부근의 해수 및 침전물, 원생동물, 어패류 등에도 널리 분포하고 있다. V. cholerae non-O1/O139의 생화학적 성상은 콜레라와 같고 TCBS 한천배지에서 sucrose를 발효하여 황색의 집락을 형성한다. V. cholerae non-O1/O139의 발육최적 온도는 30~37℃이며, 발육최적 pH는 7.6~8.4의 약알칼리이다. 산성의 환경에서는 증식하기 어렵고 pH가 4.5 이하가 되면 급속하게 사멸해 버린다. 또 저온에서도 증식하기 어려워 10℃ 이하의 환경에서는 발육할 수 없게 된다. 또 열에 대한 저항성도 약하여 60℃에서 10분간 정도 가열하면 사멸한다.
병원성 인자
콜레라의 격렬한 설사 원인물질은 콜레라균이 생산하는 cholerae toxin(CT)에 기인하지만 V. cholerae non-O1(O139는 제외) 분리균주에서 CT를 생산한 것은 약 2%로 적다. V. cholerae non-O1의 병원인자는 CT 및 CT유사 독소 외에 El Tor형 콜레라와 유사한 용혈독(El Tor hemolysin), 독소원성 대장균이 생산하는 내열성 엔테로톡신(ST)과 유사한 독소(NAG-ST), 또 장염비브리오의 내열성 용혈독소, 이질균의 시가독소 등의 생산이 알려져 있다. 그리고 이들 균이 설사를 일으키기 위해서는 우선 장관 내에 점착, 증식하는 것이 필요하며, 점착 인자로는 편모, 섬모, 혈구응집소(hemagglutinin)등이 알려져 있다. V. cholerae non-O1의 설사 메커니즘은 콜레라와 유사하다. 한편 이 균의 대부분이 대량의 El Tor hemolysin을 생산하는 것이 확인되어 El Tor hemolysin의 장관독성이 시사되었다. 토끼 장관결찰 루프시험과 마우스 위내 투여시험 등의 결과에서 El Tor hemoly -sin이 콜레라설사 이외의 원인 독소인 것으로 확인되었다. NAG-ST도 콜레라 설사 이외의 원인독소인 것이 명확하지만 이 독소를 생산하는 균주는 분리균주 전체의 1~5%정도이다.증상 및 치료
일반적으로 V. cholerae non-O1이 원인이 되어 발병하는 위장염의 증상은 다른 병원성 비브리오와 유사하다. 잠복기간은 수 시간에서 5일(통상 1~3일)이며 이 균에 감염될 경우, 설사, 메스꺼움, 구토, 열을 수반한 복통과 같은 전형적인 식중독 증상을 나타낸다. 중증의 경우는 콜레라와 같이 격렬한 설사를 동반하고 탈수증상이 일어난다. 특히 기초질환을 가진 환자에서는 패혈증으로 진전되는 경우도 있다. 치료에는 일반적인 위장염과 동일한 요법을 실시하고 탈수증상이 보이는 경우에는 수액요법을 병행한다. Norfloxacin, ofloxacin, ciprofloxacin 등의 newquinolone제는 감염균의 배균시간을 단축하는 데는 유효하지만, 소아에 사용 시는 문제가 되는 경우도 있어 주의를 요한다.비브리오 미미쿠스(Vibrio mimicus)
V. mimicus는 1981년 Davis 등에 의하여 제안된 종으로 sucrose 발효성, 그 외의 약간의 생화학적 성상이 다른 점 이외는 생태와 병원성에 있어서도 V. cholerae와 유사하고 또 혈청학적으로도 공통성이 있다. 처음에는 V. cholerae로 분류되었지만 DNA-DNA 상동성에서의 차이가 명확하여 별도의 균종으로 나누어졌다.
특징
V. mimicus는 그람음성 간균, 통성혐기성, oxidase 양성, 포도당 발효능 및 1~3%의 식염을 좋아하는 저도호염성의 특징을 갖는다. 콜레라와 같이 약간 만곡한 콤마상의 형태를 하고 있고 1개의 편모(극단모성 편모)를 갖고 있다. V. mimicus는 본래 열대와 아열대의 콜레라 유행지역에 분포하는 상재균이지만 현재는 유럽이나 우리나라, 일본 등의 도시하천, 하수, 연안 해수 및 어패류에서도 이 균이 검출되고 있다. 그러나 그 오염 상황은 하천의 전역에 분포하는 담수성 세균인 Aeromonas속 균과는 생태학적으로 다른 양상을 나타낸다. V. mimicus는 생화학적으로 sucrose 비분해 및 VP 음성이라는 점에서 V. cholerae non-O1/O139와 구별되지만 그 외의 생화학적 성상, 생태 및 병원성은 V. cholerae non-O1/O139와 유사하다. 이 균이 V. mimicus로서 분리된 점은 DNA-DNA 상동성에서의 차이에 의한 것으로 V. cholerae와 V. mimicus의 상동성은 42~48% 정도이다. V. mimicus는 sucrose을 발효하지 않기 때문에 TCBS 한천배지에서 장염비브리오와 비슷한 청록색의 집락을 형성한다. 그 집락의 크기는 장염비브리오 및 V. cholerae non-O1등과 비교하여 대체로 작은 경우가 많다.
원인식품 및 증상
근해산의 어패류가 원인식품이며, 저온(10℃ 이하)에 보존하면 발육할 수 없기 때문에 발병균수에는 미치지 못한다. 주증상은 수양성 설사, 구토, 복통이다. 치료법은 V. cholerae non-O1의 경우와 유사하다.비브리오 플루비알리스(Vibrio fluvialis)
V. fluvialis는 해수에 분포하는 호염성 비브리오 종으로 1977년에 group F 비브리오로 가칭되었다. 같은 시기 방글라데시에서의 설사증 유행에서 같은 균이 분리되어 Enteric group EF-6으로 가칭되었지만 1981년 group F 비브리오는 V. fluvialis로 명명되었으며, Enteric group EF6도 동일 균종인 것으로 확인되었다. 이 균은 생화학적 성상 중 일부의 차이에서 생물형 1과 2로 구별되었지만 그 후 DNA-DNA 상동성에서의 차이를 기본으로 생물형 1이 V. fluvialis, 생물형 2는 V. furnissi라고 하는 다른 균종 명이 부여되었다.
특징
V. fluvialis는 그람음성의 단간균으로 극단모성 편모를 가지지만 고형 배지에서는 측모 또는 주모를 생성하는 것도 있다. V. fluvialis는 발육에 식염을 요구한다. 이 균의 분리는 TCBS 한천배지, 비브리오용 한천배지를 이용하면 좋지만 확인배지에는 식염을 2~3% 첨가해야 한다. 현재 V. fluvialis는 35종류의 혈청형(O군)으로 구별되어 역학 marker로서 이용되고 있다. 이들 혈청형중 O4, O5, 및 O10은 V. cholerae 혈청형 O41, O39 및 O6과 각각 일치하는 것이 확인되었으며, 더욱이 V. fluvialis O19는 콜레라균의 항원인자를 보유한다. 따라서 V. fluvialis O19는 콜레라균 진단용 항혈청의 혼합혈청 및 이나바형 인자혈청에 응집을 나타내고 또 이 균은 TCBS 한천배지에서 sucrose의 발효에 의해 황색 집락을 형성하는 것으로 콜레라균의 감별에는 충분한 주의가 필요하다.
역학
V. fluvialis에 의한 최초의 설사증은 1975년 바렌에서 발생한 설사환자에서 분리되었다. 그 후 방글라데시에서 1976년 10월부터 다음해 6월 사이에 약 1만 명의 설사환자 중 5%에서 이 균이 분리되었다. 환자의 임상증상은 콜레라와 같은 설사였으나, 일부에서는 복통이나 발열이 있었고, 혈변을 나타낸 환자도 있었으며, 환자의 과반수는 5세 이하의 소아였다. 그 후 인도에서도 위장염 환자에서 V. fluvialis가 분리되었다. 미국에서는 심한 수양성 설사로 사망한 노인에서 분리한 예가 보고되었으며, 급성 화농성담도염이나 굴을 생식한 위장염 환자에서 분리한 예가 보고되어 있다.병원성 인자
V. fluvialis가 설사원성을 가지는 것은 토끼장관 결찰루프 시험 등의 결과에서 명확하게 나타났지만 설사의 발병기구에 대해서는 아직 충분하게 연구되어 있지 않다. 이 균의 병원인자로서는 세포독성을 가지는 이열성 독소, CT독소, hemolysin 등이 있다. 또 이 균은 protease, mutinase, phosphatase 등을 생산하지만, 이들의 물질과 설사증과의 관계는 아직 잘 알려져 있지 않다.임상증상 및 치료
V. fluvialis에 의한 위장염의 증상도 다른 균에 의한 것과 유사하여 수양성의 설사가 주증상이지만 보통은 비교적 경증이다. 때로 복통과 발열, 가벼운 혈변성 설사를 일으킨다. 잠복기간은 수 시간에서 3일 정도(보통 24시간 전후)이다. 또 위장염의 치료는 V. cholerae non-O1 및 V. mimicus의 경우와 같다고 생각해도 좋다.테트라싸이클린계 항생제
테트라싸이클린계 항생물질은 polycycle 구조를 가지고 있는 항생물질로서 클로르테트라싸이클린, 옥시테트라싸이클린 및 테트라싸이클린은 토양균에서 생성되는 항생물질을 검사하다가 발견되었으며, 데모클로싸이클린 (democlocycline), 독시싸이클린(doxycycline), 마이노싸이클린 (minocycline) 등은 근래에 소개 되었다.
테트라싸이클린계 항생물질은 광범위한 항생물질로서 많은 그람양성 및 음성세균, Rickettsiae, Mycoplasmae 및 Chlamydiae 등에 효과적이다. 그 외 Leptospira나 Treponema 같은 spirochetes 및 Entamoeba histolytica와 Plasmodium falciparum 같은 원충류(protozoa)에도 효과가 있다. 그러나 Proteus sp. 및 Pseudomonas sp.는 일반적으로 이 약물에 저항성을 가진다.
모든 테트라싸이클린계 항생물질 간에는 교차내성이 있어 한 가지 테트라싸이클린계 항생물질에 저항성이 생기면 모든 다른 테트라싸이클린계에 대해서도 저항하므로 한 가지 테트라싸이클린계만을 선택하여 사용하는 것이 바람직하다.
테트라싸이클린계 항생물질은 광범위한 항생물질로서 많은 그람양성 및 음성세균, Rickettsiae, Mycoplasmae 및 Chlamydiae 등에 효과적이다. 그 외 Leptospira나 Treponema 같은 spirochetes 및 Entamoeba histolytica와 Plasmodium falciparum 같은 원충류(protozoa)에도 효과가 있다. 그러나 Proteus sp. 및 Pseudomonas sp.는 일반적으로 이 약물에 저항성을 가진다.
모든 테트라싸이클린계 항생물질 간에는 교차내성이 있어 한 가지 테트라싸이클린계 항생물질에 저항성이 생기면 모든 다른 테트라싸이클린계에 대해서도 저항하므로 한 가지 테트라싸이클린계만을 선택하여 사용하는 것이 바람직하다.
용도
테트라싸이클린계 항생물질이 처음 소개되었을 때는 광범위한 항균작용을 가지고 있어 널리 사용되었으나, 최근에는 점차 그 용도가 적어져서 제1차 약물로서는 다음과 같은 경우에 사용된다. 즉, 콜레라 치료에는 아직까지 많이 사용되며, Rickettsia 및 Coxiella 감염, 서혜부육아종(granuloma inguinale), 야토병(tularemia), Chlamydia 감염(trachoma, lymphogranuloma venereum 및 psittacosis) 또는, 비특이성 요도염 등에 일차 약물로서 사용되고 있다. 또한 Brucella, Pasteurella 및 Mycoplasma 감염 질환에도 많이 사용된다.그 외 매독, 연성하감(chancroid), 임질, 방선균증(actinomycosis), 이질(shigellosis) 등에 2차적으로 선택되어 쓰이고 있다. 임상적으로 테트라싸이클린계 항생물질은 여드름(acne) 치료에 소량을 장기간 투여할 경우 효과적이며, 이는 피지(sebum) 중의 지방산 농도를 감소시키기 때문이라고 한다. 그 외에 Whipple병, 열대성 스프루우(tropical sprue), 만성기관지염 및 요로감염 등에 사용되기도 한다.
모든 테트라싸이클린계 항생물질은 서로 비슷한 작용과 효능을 가지고 있으나, 그 중 독시싸이클린은 반감기가 길고 신장독성이 없으므로 신장장애 환자에 애용되고 있다. 수산용 약품으로서 옥시테트라싸이클린은 방어의 비브리오병, 연쇄상구균병, 뱀장어의 기적병, 에드와드병, 아가미부식병, 잉어의 솔방울병, 아가미부식병, 송어의 비브리오병, 절창병 등의 치료에 효능이 있고 독시싸이클린은 어류의 연쇄상구균증 및 연쇄상구균증의 치료에 효과가 있다.
위해성
가장 흔히 나타나는 부작용으로는 테트라싸이클린계 항생물질의 내복에 의한 소화기 계통의 증상이다. 즉, 오심, 구토, 상복구 통증, 설사 등이 흔히 나타나고 구강염 및 설염도 가끔 나타나기도 하며, 정맥주사 하였을 때는 정맥염을 일으키기도 한다. 테트라싸이클린계 항생물질은 간장독성을 가지고 있으며, 특히 신장장애 환자에서 자주 나타난다. 또한 신장독성도 가지고 있으므로 신장독성을 가진 다른 약물과 같이 사용하지 않도록 하여야 한다. 또한 피부발진, 발열 등의 알레르기반응이 드물게 나타나기도 하며, 독시싸이클린은 광과민(photosenstivity)을 일으키기도 한다.또한, 테트라싸이클린계 항생물질은 광범위 항균제이므로 Candida albicans 및 Staphylococcus aureus에 의한 중복감염을 나타내기도 한다. 유아 및 소아에 테트라싸이클린계 항생물질을 투여하였을 때 치아 및 뼈가 황갈색으로 변하는 현상이 나타나며, 이것은 테트라싸이클린계 항생물질이 석회화(calcification)가 활발한 곳에 침착되기 때문이다. 따라서 임신 4개월이 지난 임산부 및 소아에는 테트라싸이클린계 항생물질을 투여하지 않도록 하여야 한다. 유효기간이 경과하였거나, 분해된 테트라싸이클린계 항생물질을 내복 하였을 때는 신세뇨관의 장애를 일으켜 판코니(Fanconi) 증후군이 나타날 수 있다. 판코니증후군은 오심, 구토, 산혈증, 단백뇨, 당뇨 및 아미노산뇨 등의 임상적 증상이 나타나며, 이런 증상은 약물투여를 중단하면 1개월 이내에 없어진다.
국내외 관리현황
| 항생제명 | 기준치 | 대상 수산물 |
|---|---|---|
| [식품의약품안전처, 2020] | ||
| 옥시테트라싸이클린(Oxytetracycline), 클로르테트라싸이클린(Chlortetracycline), 테트라싸이클린 합계(Tetracycline) |
0.2 mg/kg | 어류, 갑각류, 전복 |
| 독시싸이클린 | 0.05 mg/kg | 어류 |
퀴놀론계 및 플루오로퀴놀론계 항생제
-
퀴놀론계 항생제
물, 에탄올, 무수에탄올에 녹지 않고 알칼리성 수용액 (수산화나트륨액, 개미산)에 잘 녹는 성질을 가진다. 퀴놀론계 항생제는 서로 유사한 활성기인 pyridone carboxylic acid를 가지고 있으며, 4-quinolone nucleus와 3번 위치의 carboxyl기를 공통으로 가지고 있다. 특히 옥소린산은 7, 8번 위치의 methylenedioxy기에 의해 다른 퀴놀론계 항생제들과 구별되어진다. 퀴놀론계 항생제는 병원성 세균의 핵에 직접 작용하여 DNA 합성에 관여하는 DNA 복제의 기능을 저해하여 세포분열을 억제함으로써 독특하게 살균효과를 나타내고, 세균의 표면에 존재하는 섬모는 숙주의 상피조직에 부착하려는 성질이 있는데, 이 섬모를 표면에서 완전히 탈락시켜 병원성 세균이 숙주의 조직에 부착하지 못하게 함으로써 효과를 나타낸다. 또한, 이들은 기타 항생제와 설파제 등에 내성이 생긴 세균에 대하여도 우수한 항균력을 발휘하며 자체 내성은 물론이고 이들과의 교차내성도 없는 항생제로 알려져 있다. 뿐만 아니라 생체 내에서의 배출속도가 기존의 항생제 보다 빠른 것으로 보고되고 있다. -
루오로퀴놀론계 항생제
퀴놀론계 항생제는 1962년 nalidixic acid가 최초로 발견된 이래 항균 범위와 항균력을 개선하기 위하여 quinoline을 기본구조로 하는 합성물들이 만들어져, 25개 이상의 유도체들이 합성되어져 왔으며, 이후 이들 제제의 효능을 개선하여 quinoline의 6번 탄소위치에 불소 (F)를 첨가함으로써 항균력의 범위가 더욱 넓어진 2세대 퀴놀론인 플루오로퀴놀론 (fluoroquinolone)계 항균제가 개발되었다. 특히, 플루오로퀴놀론계는 서로 유사한 활성기인 pyridone carboxylic acid를 가지며, 4-quinolone nucleus와 3번 위치의 carboxyl기를 공통으로 가지고 있다. 또한 6-fluoro와 7-piperazino기를 가지며, 1-nitrogen 및 piperano기의 변화에 따라 다양한 유사구조를 가지고 있다.
퀴놀론계의 작용기전에 대해서는 정확하게 밝혀져 있지는 않으나 세균의 DNA gyrase 작용을 억제하여 DNA 복제 및 핵전사를 포함한 다양한 세포 기능을 방해함으로써 항균력을 갖는 것으로 알려져 있으며, Pseudomonas, Haemophilus, Campylobacter와 같은 그람 음성세균과 Streptococci, Staphylococci 등 그람양성세균 모두에 대한 탁월한 효과를 가진 것으로 보고되어 있다. 또한 퀴놀론계 항생제는 경구투여로 비교적 체내에 잘 흡수되어 전신 체액과 조직에 골고루 분포하며, 주로 간이나 신장을 통한 대사에 의해 N-oxide, oxo-, glucuronide 또는 demethylation 된 형태로 혈액 내에 존재하거나 뇨로 배출된다. 또한 낮은 독성과 넓은 항균범위로 인하여 임상에 많이 사용하고 있으며 소변, 폐 내에 고농도로 존재하기 때문에 비뇨 기계, 호흡기계 질병에 적용하며 또한 소화기, 피부 등의 감염에도 다양하게 적용하였다.
용도
퀴놀론계의 약물은 항말라리아제인 클로르퀸을 합성하는 과정 중에 증류물로 부터 분리한 1, 8-naphthyridine, 즉 nalidixic acid가 그 효시이며, 1984년 미국 식품의약품안전청으로부터 시판허가를 받은 불소화된 퀴놀론인 norfloxacin의 개발 이후 그 가치를 인정받게 되었다. 이 항균 물질은 1980년대 초기에 처음 우리나라 어류양식업계에 소개되면서 그 사용이 점차 증가하기 시작하여 현재 어류질병 치료에 중요한 항균물질로 대두되었다. 퀴놀론계 항균물질 중 플루오로퀴놀론계 (new quinolones)는 기존의 퀴놀론계 (old quinolones)보다 더욱 광범위한 항균 물질로 그람 양성세균까지도 항균력을 발휘하였다. 이는 어류의 세균성 질병의 치료에 대해 매우 효과적으로 최소발육 억제농도 (MIC)가 Pasteurella piscicida, Vibrio anguillarum, Edwardsiella tarda, Streptococcus sp.에 대해서 초기의 것 (old quinolones)보다 더 낮으며, 낮은 농도로서 뛰어난 감수성을 나타내고 있었고, Aeromonas salmonicida에 감염된 연어를 약욕함으로써 치료효과가 있음을 보고하였다.2008년 7월 1일부터 플루오로퀴놀론계 항생제는 약사법 제 76조 및 85조에 의거하여 국내 제조 및 수입금지 조치되어 제품으로 판매가 금지되었다. 수산용 옥소린산은 방어의 유결절증, 뱀장어의 지느러미부식병, 아가미부식병, 에드와드병, 적점병, 잉어의 궤양병, 에로모나스병, 송어의 비브리오병, 절창병 등의 치료에 효능이 있고 플루메퀸은 방어의 유결절증, 무지개송어의 절창병, 뱀장어의 에드와드병 등의 치료에 효능이 있다.
위해성
퀴놀론계 항생제의 일반적인 증상은 오심, 구토, 복통 등이 흔히 나타나는 부작용이며, 알레르기반응으로 피부 발진, 호산구증 등이 나타나며 때로는 광과민 (photosensitivity)도 나타난다. 이외에 말초신경염, 시력장애, 혈액장애, 황달 등도 보고되고 있고, 중추신경 장애증상도 나타난다. 플루오로퀴놀론계 약물의 인체에 대한 독성은 아직 명확히 알려져 있지는 않으나 prokaryotes에서만 발견되는 type Ⅱ topoisomerase인 DNA gyrase를 억제하는 것과 관련되는 것으로 보고되고 있다.국내외 관리현황
| 항생제명 | 기준치 | 대상 수산물 |
|---|---|---|
| [식품의약품안전처, 2020] | ||
| 옥소린산 (Oxolinic acid) | 0.1 mg/kg | 어류, 갑각류 |
| 플루메퀸 (Flumequine) | 0.5 mg/kg | 어류, 갑각류 |
| 날리딕스산 (Nalidixic acid) | 0.03 mg/kg | 어류 |
| 노르플록사신 (Norfloxacin) | 불검출 (정량한계 0.7 μg/kg) | 어류, 갑각류 |
| 오플록사신 (Ofloxacin) | 불검출 (정량한계 0.2 μg/kg) | 어류, 갑각류 |
| 페플록사신 (Pefloxacin) | 불검출 (정량한계 0.7 μg/kg) | 어류, 갑각류 |
| 엔로플록사신, 시프로플록사신 합계 (Enrofloxacin, ciprofloxacin) | 0.1 mg/kg | 어류, 갑각류 |
| 디플록사신 (Difloxacin) | 0.3 mg/kg | 어류, 갑각류 |
마크로라이드계 항생제
-
스피라마이신
스피라마이신 (Spiramycin)은 방선균인 Streptomyces ambofaciens로부터 개발한 마크로라이드계 항생제로서 에리스로마이신과 비슷한 항균범위를 가지며, 추천 용량에서의 혈중농도도 비슷한 수치를 보인다. 그러나 실험동물 및 사람을 대상으로 한 시험에서 스피라마이신은 에리스로마이신, 암피실린, 테트라싸이클린 보다 높고 지속적인 조직농도를 보이며, 또한 타액 내에서의 살균농도는 혈중 농도를 훨씬 상회한다. 이와 같이 스피라마이신은 기도조직에 친화성을 보이며, 타액 및 폐조직에 고농도로 분포한다. 특히, 연쇄구균 및 폐렴구균의 MIC 이상으로 타액 내에서 45시간가량 살균농도를 지속하므로 기도 감염증의 성공적인 치료를 기대할 수 있는 약물이다.
스피라마이신은 3개의 당이 결합된 16원환의 lactone ring을 함유하며, 당 중 2개는 서로 연결되어 있다. 이것은 3개의 화학적 구조가 관련되어 있는 스피라마이신 Ⅰ, Ⅱ, Ⅲ의 염기 혼합물이다. 스피라마이신은 물에 약간 용해되고, UVmax (ethanol)는 231 ㎚이며, 대부분의 유기용매에 녹는다.수산동물용 스피라마이신은 경구투여에 의하여 급속히 흡수되는데 혈액 및 장기 내 농도는 투여 후 3~6시간에 가장 높으며, 그 후 서서히 체외로 배출 되어 근육에서는 10일, 기타 혈액, 간장, 신장, 비장 등에서는 14일 후에 완전히 소실된다고 한다. 단백 결합율은 20% 정도로 작으며, 스피라마이신의 흡수속도는 에리스로마이신 등 다른 제제와 비교하면 다소 느린 경향이 있지만, 스피라마이신은 hemiketal을 형성하지 않으며, 긴 post-antibiotic effect를 가짐으로써 위장에서 안정하며, 지속적인 효과를 나타낸다. 주로 그람 양성세균에 작용하며, 그람음성 혐기성 균에 내성을 보인다. 일반적으로 혈장농도에서 정균작용을 나타내며 조직농도가 높아지면 살균작용을 나타내기도 한다. 포도상구균, 연쇄상구균, 폐렴구균, 임균, 매독 트레포네마, 톡소플라스마, 수막염균, 백일해균, 코리네박테리움, 리스테리아속, 클로스트리듐, 마이코플라스마, 클라미디아, 레지오넬라, 펩토스피라, 캄필로박터속, 헤모필루스 인플루엔자에 대하여 효과를 나타낸다.스피라마이신 Ⅰ : C43H74N2O14 결정형 R=H, mp: 134-137°[α]20D : -96°
스피라마이신 Ⅱ : C45H76N2O51 결정형 R=COCH3, mp: 130-133°[α]20D : -86°
스피라마이신 Ⅲ : C46H78N2O15 결정형 R=COCH2CH3, mp: 128-131°[α]20D : -83°
-
에리스로마이신
에리스로마이신은 물에 잘 용해되지 않으며, 엷은 황색의 결정 또는 분말로서 냄새는 없거나 거의 없고 맛은 쓰며, 흡습성을 가지고 있는 항생제이다. 이 항생제는 마크로라이드계 항생제로 큰 lactone ring 당이 결합되어 있으며, Streptomyces erythreus의 균주에서 분리된 항생제로 분자량이 약 700인 유기염기이다. 에리스로마이신은 특히 그람 양성세균에 강한 살균작용을 일으키고 항균범위는 페니실린과 테트라싸이클린의 중간정도이고 대장균 및 salmonella 등과 같은 그람 음성간균에는 효과가 그다지 없다. 에리스로마이신의 흡수경로는 위산에 의하여 잘 파괴되기 때문에 염의 형태나 에스테르의 형태로서 경구투여되며, 혈장내에서는 체조직 속으로 즉시 들어가 폐, 신장, 간 및 타액선에서 높은 농도를 이른다. 또한 간에 의해서 변환되며 주로 담즙 속으로 배출되거나 뇨 속으로도 배출되나 뇨 속에서도 활성 형태의 것이 높은 농도를 이룬다.
용도
수산동물용 스피라마이신은 방어, 은어, 틸라피아에 대하여는 연쇄구균증에 탁월한 효과를 나타내며, 잉어, 무지개송어, 뱀장어, 방어의 경우 아가미 부식병 또는 비브리오병에 대하여 효과가 있는 것으로 알려져 있다. 에리스로마이신은 넙치, 조피볼락, 돔류의 연쇄구균증, 점상출혈증, 노카르디아병, 송어, 연어의 세균성 신장병, 연쇄상구균증 뱀장어, 틸라피아의 연쇄상구균증 치료에 효능이 있다.위해성
스피라마이신이 사용된 후에 나타난 부작용으로는 오심, 구토, 설사 및 피부과민 등이 보고되고 있다. 반면 에리스로마이신은 다른 항생제에 비하여 위해성은 적다. 에리스로마이신을 내복할 경우 오심, 구토, 설사 및 복통 등의 소화기계통 장애증상이 흔히 나타나고 드물지만 과민반응으로 발열, 피부발진, 호산구 증가증 (eosinophilia) 등도 나타나고 정맥주사로 혈전성 정맥염 (thrombophlebitis)이 생기기도 한다.국내외 관리현황
| 항생제명 | 기준치 | 대상 수산물 |
|---|---|---|
| [식품의약품안전처, 2020] | ||
| 스피라마이신 (Spiramycin) | 0.2 mg/kg | 어류, 갑각류 |
| 에리스로마이신 (Erythromycin) | 0.2 mg/kg | 어류, 갑각류 |
| 조사마이신 (Josamycin) | 0.05 mg/kg | 어류 |
| 키타사마이신 (Kitasamycin) | 0.2 mg/kg | 어류 |
페니실린계 항생제
백색 또는 거의 백색의 결정성 분말이며, 냄새는 거의 없다. 또한 알콜 및 메틸알콜에 용해되지 않으며, 클로로포름, 에테르에는 거의 녹지 않고, 물, 산 용액 및 알칼리수산화물의 묽은 용액에 녹는 성질이 있다. 이 페니실린계의 항생제는 β-lactam ring과 thiazolidine ring으로 구성된 6-amino penicillanic acid를 기본 구조핵으로 가지고 있는 유기산으로서 이에 각종 화합물로 구성된 측쇄 (R)와 결합되어 있으며, 결합된 측쇄에 따라 항균범위, 산 (acid)에 대한 안정성, 흡수율 등이 달라질 수 있다.
용도
모든 페니실린계 항생제는 같은 작용기전, 즉 세균 세포벽의 합성을 방지하여 살균작용을 일으키며, 그람양성구균 및 황색포도상구균에 예민하게 작용할 뿐만 아니라 그람음성간균에 특히 효과가 있다. 또한 수산용 약품으로서도 어류 양식업계에서 어류질병인 유결절증, 절창병의 치료제로 사용하고 있다. 특히, 아목시실린은 뱀장어의 지느러미적병, 송어의 비브리오병, 방어의 유결절증 등의 치료에 효능이 있으며, 임피실린은 방어의 유결절증, 송어의 절창병, 뱀장어의 에로모나스병 등의 치료에 효능이 있다.위해성
페니실린계 항생제는 직접독성은 극히 경미하나 대량 장기간 투여할 때 과민반응을 일으키며, 특히 뇌척수강내 (intrathecal)로 투여할 경우 신경독성으로 전신경련을 나타내기도 한다. 그 외 설염 (glossitis) 및 구각염 (stomatitis), 간기능 이상, 백혈구 감소, 신장독성 등이 드물게 생기며, 암피실린 및 아목시실린을 내복하였을 때에는 종종 설사가 나타나고, Candida albicans의 중복감염이 문제되기도 한다.국내외 관리현황
| 항생제명 | 기준치 | 대상 수산물 |
|---|---|---|
| [식품의약품안전처, 2020] | ||
| 아목시실린 (Amoxicillin) | 0.05 mg/kg | 어류, 갑각류 |
| 암피실린 (Ampicillin) | 0.05 mg/kg | 어류, 갑각류 |
클로람페니콜계 항생제
클로람페니콜계 항생제는 대부분 쓴맛이 나는 무취의 백색 또는 황백색의 결정이며, 냄새는 없고, 물에 약간 녹으며 알콜 및 아세톤 등에는 잘 녹지 않는 성질이 있다. 그중에서 클로람페니콜은 그람음성 및 그람양성 박테리아, 리케치아, 클라미디아 및 마코플라스마에 대하여 뛰어난 항균작용이 있으며 특히 장티푸스균 (Salmonella typhi) 및 헤모필루스 인플루엔자 (Haemophilus influenzae)가 유발하는 감염에 효과적으로 작용하는 구세대 광범위 항생제 중 하나이다. 치암페니콜과 플로르페니콜 역시 비슷한 광범위 항균효력을 가지고 있으나 클로람페니콜보다는 항균력이 약하다. 이들 클로람페니콜계 항생제는 소화기계통에서 신속히 흡수되며, 주로 뇨 속에 배출되기도 하고, 담즙 속으로 배출되기도 한다.
용도
수산용 약품으로서 치암페니콜은 방어의 비브리오병, 유결절증, 송어의 비브리오병, 절창병, 은어의 비브리오병, 방어 및 광어의 유결절증, 비브리오병, 연쇄상구균증, 틸라피아의 슈도모나스병, 비브리오병 등의 치료에 효과가 있으며, 플로르페니콜은 방어의 유결절증, 연쇄상구균증, 뱀장어의 에드와드병, 송어의 절창병, 비브리오병, 은어의 비브리오병 등의 치료에 효과가 있다.위해성
클로람페니콜은 가장 잘 알려진 위해로 사람에 있어서 재생불량성 빈혈 (aplastic anemia)을 일으키며, 이는 용량에 관계없이 특이체질성으로 나타나 치명적이기도 하나 그 원인은 아직 밝혀지지 않은 것으로 알려져 있다. 그래서 이후 개발된 항생제가 치암페니콜과 후로르페니콜이며, 효력은 약하나 재생 불량성 빈혈을 일으키지 않는 안전성이 크다는 장점을 가지고 있다.국내외 관리현황
| 항생제명 | 기준치 | 대상 수산물 |
|---|---|---|
| [식품의약품안전처, 2020] | ||
| 아목시실린 (Amoxicillin) | 0.05 mg/kg | 어류, 갑각류 |
| 암피실린 (Ampicillin) | 0.05 mg/kg | 어류, 갑각류 |
설파제계 항생제
설파제계의 물질들은 대부분 백색 또는 담황백색을 띠는 결정 또는 결정성분말로서 냄새는 없고 맛은 약간 쓰다. 또한 개별 항생제마다 다르지만, 빛에는 변하는 성질을 가지고 있고, 물에는 대부분 잘 녹고, 유기용매에는 잘 녹지 않는다. 설파제계 중에서 가장 효력이 강하고 반면에 위해성도 적은 약물이 sulfadiazine이며, sulfamerazine과 sulfamethazine도 sulfadiazine과 비슷하나 배설이 다소 느리고, 혈장 단백질과의 결합이 다소 강하며, 이 세 약물을 혼합하면 triple sulfonamide mixture 혹은 sulfapyrimidine이라고 하여 신장에 대한 독작용을 감소시키고 효력을 증가시킬 목적으로 사용한다. 트리메토프림 (trimethoprim)은 dihydrofolic acid와 비슷한 구조를 가지고 있으며, dihydrofolic acid를 환원하여 tetrahydrofolic acid로의 전환을 촉매하는 효소인 dihydrofolate reductase를 상경적으로 억제함으로써 염산의 환원을 억제한다.
용도
설파제계는 광범위 항균제에 속하며, 대부분이 그람 양성세균과 일부 그람 음성구균 (cocci) 및 간균 (bacilli), 방선균 (actinomycetes), Chlamydiae 및 원충류 (protozoa)에도 효과가 있다. 또한, Toxoplasma gondii와 chloroquin에 저항성을 지닌 Plasmodium falciparum의 감염질병에도 사용한다. 수산용 약품으로 설파디메톡신은 무지개송어의 비브리오병, 방어의 비브리오병, 유결절증 치료에 효과가 있으며 설파모노메툭신은 뱀장어의 지느러미적병, 송어의 비브리오병, 절창병, 궤양병, 아가미부식병, 잉어의 솔방울병, 방어의 비브리오병 치료에 효과가 있다.위해성
설파제계는 비교적 안전한 약물이나, 때로는 과민반응이 나타난다. 그 증상으로는 피부발진, 발열 등으로부터 심한 알러지 반응으로 맥관염 (vasculitis), 무과립백혈구증 (agranulocytosis) 및 혈소판 감소증 (thrombocytopenia) 등이 나타나기도 한다. 또한 Stevens-Johnson 증후군 (발열, 무력증과 구강 및 음부점막의 궤양을 동반하는 다발성 홍반이 특징적으로 나타남)도 나타나며 일광과민 반응이 나타나기도 한다. 특히 트리메토프림의 경우 피부발진, 중추신경장 등이 나타나며, trimethoprim은 sulfamethoxazole의 혈액상 및 위상계 독성을 증강시킨다.국내외 관리현황
| 항생제명 | 기준치 | 대상 수산물 |
|---|---|---|
| [식품의약품안전처, 2020] | ||
| 설파제 [Sulfonamides의 총합] | 0.1 mg/kg | 어류 |
| 트리메토프림(Trimethoprim) | 0.05 mg/kg | 어류, 갑각류 |
| * 설파제 총합: 설파구아니딘(Sulfaguanidine), 설파독신(Sulfadoxine), 설파디메톡신(Sulfadimethoxine), 설파디아진(Sulfadiazine), 설파메라진(Sulfamerazine), 설파메타진(Sulfamethazine, Sulfadimidine), 설파메톡사졸(Sulfamethoxazole), 설파메톡시피리다진(Sulfamethoxypyridazine), 설파모노메톡신(Sulfamonomethoxine), 설파퀴녹살린(Sulfaquinoxaline), 설파클로르피리다진 (Sulfachlorpyridazine), 설파클로진 (Sulfachlorpyrazine, Sulfaclozine), 설파티아졸(Sulfathiazole), 설파페나졸(Sulfaphenazole), 설피속사졸(Sulfisoxazole)의 합 | ||
아미노글리코사이계 항생제
아미노글리코사이드계 항생제는 두개 혹은 그 이상의 아미노당 (amino-sugar)이 배당체성 결합 (glycosidic linkage)으로 중심부의 육탄당 핵 (hexose nucleus)에 연결되어 있다. 이 hexose nucleus는 화학적으로 aminocyclitol로서 streptomycin에서는 streptidine이고, 기타 항생제에서는 2-deoxystreptamine이다. 그러므로 이들 항생제는 화학구조상 aminoglycosidic aminocyclitols로서 간단히 aminoglycoside 항생제라고 부르고 있다. 모든 아미노글리코사이드계 항생제는 서로 비슷한 항균범위를 가지고 있으며 그람 음성 장내세균 및 포도상 구균에 가장 강력한 항균작용을 나타내고 결핵균 (Mycobacterium tuberculosis)은 streptomycin, gentamicin에 예민한 감수성을 가지고 있다. 그람 양성세균 중에서 특히 황색 포도상구균 (Staphylococcus aureus)도 아미노글리코사이드계 항생제에 예민하다. 그러나 혐기성 세균은 일반적으로 저항성을 지닌다.
용도
수산용 약품으로서 겐타마이신은 잉어의 에로모나스, 궤양병, 송어의 콜룸나리스병, 넙치의 비브리오병, 연쇄상구균증, 에드와드병 등의 치료에 효과가 있으며, 네오마이신은 어류의 기적병, 에드워드병 치료에 효과가 있다.위해성
아미노글리코사이드계 항생제는 안전한계 (safety margin)가 좁은 약물로서 즉, 치료량 (therapeutic dose)과 중독량 (toxic dose)과의 사이가 좁다. 가장 흔히 보고되는 독작용으로서는 신장독성과 이독성 (ototoxicity)이며 이독성의 증상으로는 이명 (tinnitus), 난청 (deafness), 어지러움 (vertigo) 및 보행곤란 등이며, 고주파 (high-frequency) 난청이 비교적 흔하나 상당히 심한 청력장애까지 진행되지 않는 한 발견하기 힘들다. Streptomycin, gentamicin은 주로 전정기능 (vestibular function)을 장애하고 neomycin은 주로 청력장애을 일으킬 수 있으며 그 외의 독성은 심하지 않으며 발열 및 피부발진 등을 볼 수 있다.국내외 관리현황
| 항생제명 | 기준치 | 대상 수산물 |
|---|---|---|
| [식품의약품안전처, 2020] | ||
| 겐타마이신(Gentamicin) | 0.1 mg/kg | 넙치, 송어, 잉어 |
| 네오마이신(Neomycin) | 0.5 mg/kg | 어류, 갑각류 |
린코사마이드계 항생제
린코마이신은 Streptomyces lincolnensis에서 산출된 항생제이며, 클린다마이신은 린코마이신의 7-deoxy, 7-chloro 유도체로서 린코마이신보다 항균작용이 강력하고 소화관내에서의 흡수가 양호하며 부작용이 적다. 린코마이신과 클린다마이신의 작용기전은 이들이 50 S ribosomal subunit에 결합하여 단백질 합성을 억제한다. 그 결합부위는 chloramphenicol 또는 에리스로마이신의 결합부위와 같거나 근접부위라고 한다. 이들 항균범위는 연쇄상구균, 포도상구균 및 대부분의 혐기성 세균에 효과적이나 장내구균 (enterococci)은 이에 저항하는 특징이 있으며, 소화관에서 잘 흡수하고 특히 클린다마이신은 흡수된 약물의 약 90%는 현장단백과 결합하며 대부분의 조직 특히 골조직에 잘 투과된다. 또한 간장에서 대사되어 신장으로 배설된다.
용도
수산용 약품으로 린코마이신은 방어의 연쇄상구균증의 치료에 효과가 있고 클린다마이신은 뱀장어, 넙치의 궤양병, 비브리오병, 연쇄상구균증의 치료에 효과가 있다.위해성
가장 흔히 나타나는 피부발진과 복통, 구토, 설사 등 소화기 계통의 자극증상이 나타나며 일부는 위막성 결장염 (pseudomembranous colitis)이 발생하기도 하여 대장절제 (colectomy)가 필요하기도 하고 때로는 치명적이기도 한다. 이같이 대장염은 클린다마이신에 저항성을 지닌 Clostridium difficile 균주에서 산출되는 독소에 의한 것이라고 하며, 이 Clostridium difficile은 반코마이신에 감수성이 높다.국내외 관리현황
| 항생제명 | 기준치 | 대상 수산물 |
|---|---|---|
| [식품의약품안전처, 2020] | ||
| 린코마이신(Lincomycin) | 0.1 mg/kg | 어류, 갑각류 |
| 클린다마이신(Clindamycin) | 0.1 mg/kg | 뱀장어, 넙치 |
말라카이트 그린
말라카이트그린 (Malachite Green, C23H25ClN2)은 아닐린그린, 벤즈알데히드그린, 빅토리아그린 B, 차이나그린이라고도 하며 밝은 청록색의 염기성 염료로서 트리페닐메탄계 염료의 일종이다. 벤즈알데히드 1 분자와 디메틸아닐린 2 분자를 황산 또는 염산으로 축합시켜 류코염기의 테트라메틸디아미노트리페닐메탄을 만든 후, 이것을 과산화납으로 산화하면 염료가 수산염의 결정으로 산출된다. 광택이 나는 녹색 결정으로 물과 알코올에 녹는다. 말라카이트그린은 염색약의 형태인 chromatic form으로 주로 존재한다. 그러나 말라카이트 그린이 체내에 흡수되면 대사되어 먼저 carbinol form으로 변화되는데 이 형태는 세포막을 보다 빠르게 통과한다. 다음으로 세포 내에서 carbinol form이 대사되어 류코말라카이트 그린으로 변화되며 이 형태가 말라카이트 그린의 chromatic form보다 보다 오래 머물게 됨으로써 독성을 나타내게 된다.
용도
말라카이트그린은 진균과 그람양성세균에 효과가 있다. 양어 (養魚)산업에서는 물에 사는 곰팡이로 생선의 알이나 어린물고기를 죽이는 물곰팡이속 (Saprolegnia)을 억제하는데 사용되었다.위해성
말라카이트 그린은 주로 염료로 사용되며, 임상치료에는 사용되지 않는다. 그러나 수산업계에서는 물곰팡이 제거제로서 사용되었다가 발암성 물질로 구분되어 금지시킨 물질이다. 따라서 외국의 경우도 말라카이트 그린을 1949년부터 미국 및 유럽, 일본 등 여러 나라에서 연어, 송어의 부화난에 기생한 물곰팡이를 제거하는 목적으로 사용되었다가 미국 (1991), 유럽 (2002), 일본 (2003)에서는 발암성물질로 알려져 식용 어류에서는 사용을 금지하였다.국내외 관리현황
| 항생제명 | 기준치 | 대상 수산물 |
|---|---|---|
| [식품의약품안전처, 2020] | ||
| 말라카이트 그린(Malachite green) 및 대사물질 | 불검출 (정량한계 2 μg/kg) | 축산물 및 동물성 수산물 |
니트로퓨란계 항생제
니트로퓨란계는 5-nitro-2-furaldehyde 유도체로서 그중 일부는 세균성 감염치료에 사용되고 있으며 흔히 사용되는 유도체의 아래와 같다. 나트로퓨란의 항균기전은 확실치 않으나 세균 및 포유동물세포에 있는 효소계를 억제하는 것으로 추측되고 있으며, 이 약물은 사람의 간장에서 신속히 파괴되어서 충분히 혈액농도에 달하기 어렵기 때문에 세균에만 선택적으로 독성이 강하다고 한다.
용도
니트로퓨란계는 광범위 항균제로서 대부분의 그람 양성 및 음성세균에 효과가 있다. E. coli, Klebsiella, Enterobacter, Salmonella, Shigella 및 콜레라균, 포도상구균 및 장내구균 등이 모두 예민하게 억제되나 대부분의 Proteus속 세균 및 Pseudomonas aeruginosa는 니트로퓨란계에 저항성을 지닌다.위해성
니트로퓨란계 항생제는 실험동물에서 유전자변이, 염색체등을 유발하는 변이원성이 있고, 갑상선종 등 암을 유발하는 발암성, 기형, 유산 등을 초래하는 생식독성, 난소위축, 정자수 감소등 을 초래하는 내분비계 교란성 등이 있는 것으로 보고되고 있다. 니트로퓨란계 항생제가 발암물질이라는 것이 밝혀지고, 축.수산 식품 내 잔류에 의한 인체발암성 등이 우려됨에 따라 유럽연합(EU), 미국, 일본 등 선진 각국은 1990년대 중반부터 푸라졸리돈 등 일부 물질에 대한 사용규제를 시작하였다.국내외 관리현황
| 항생제명 | 기준치 | 대상 수산물 |
|---|---|---|
| [식품의약품안전처, 2020] | ||
| 니트로퓨란(Nitrofuran)계(푸라졸리돈, 푸랄타돈, 니트로푸란토인, 니트로빈) 제제 및 대사물질 | 불검출 | 축산물 및 동물성 수산물 |
멜라민
멜라민은 백색의 결정성 고체로서 물, 에테르 및 벤젠에 녹지 않은 성질을 가지고 있다. 멜라민은 분자내에 3개의 아민 (amine) 작용기 (-NH3)를 가지고 있어 수용액은 약한 염기성을 띄며 분자내에 6개의 질소 원자를 가지고 있어 전체 분자량 중 질소가 분자량의 66%를 차지한다. 멜라민의 제조과정 중에는 시아뉼산, 아멜린, 아멜라이드 등 멜라민 유사체가 불순물로 생성된다. 그리고 살충제인 시로마진 (cyromazine)을 포유동물이 섭취했을 때 대사체로 멜라민이 생성되며 식물에서 또한 시로마진은 멜라민으로 전환된다.
위해성
멜라민의 생체내 반감기는 약 3시간으로 대부분 신장을 통해 뇨로 배설되며 설치류에 경구투여 시 반수 치사량 (LD50)은 식용 소금과 유사한 수준인 3.2 g/kg 이상으로 독성이 낮다. 유전독성은 나타나지 않고 생식기 및 피부자극에도 영향이 없는 것으로 알려져 있으며, 발암성에 대해서는 명확한 증거가 없어서 국제암연구소 (IARC)에서 그룹 3으로 분류하고 있다. 주로 방광 및 신장에 영향을 나타내는 것으로 보고되어 있으며 많은 양의 멜라민을 오랫동안 섭취할 경우 방광결석 및 신장결석 등을 유발할 수 있다.국내외 관리현황
| 항생제명 | 기준치 | 대상 수산물 |
|---|---|---|
| [식품의약품안전처, 2020] | ||
| 멜라민 (Melamine) | 2.5 mg/kg | 일부식품 (영유아 및 성장기 조제식, 조제우유 및 조제분유 등)을 제외한 모든 식품 및 식품첨가물 |
납
금속 중에서 가장 비중이 큰 물질이며, BC 1500년경부터 인류에 의해 사용되어진 가장 역사가 긴 중금속 중의 하나이며 지구의 표층에 비교적 풍부하다. 납은 주기율표 제 14족에 속하는 탄소족원소로, 자연 속에는 주로 아연광의 황화물, 황산연광, 흑연광 등의 광물로 존재한다. 지각 중 납의 평균 함유량은 13 mg/kg이며 토양 중에는 비교적 미량 존재한다. 또한 하천수 중에는 저질, 공장폐수, 광산폐수 등에 의해 용존 되어 있다. 납은 부드럽고, 매우 순응성이 뛰어나고, 유연하여 가공이 쉬울 뿐 아니라 색깔조성이 잘 된다는 이점이 있어 축전 열기, 탄약, 배관, 스크린의 빛 반사 방지, 주석을 주재료로 한 용접 합금, 페인트 안료, 도자기 유약, 포장지, 화장품, 학용품 등 산업계에서 다양하게 이용됨으로써 항상 주목되어지는 유해금속이다.
발생원
납은 자연계에 존재하는 기본적 원소로, 화합물로부터 분해되어 환경에 노출되었을 때도 그 독성이 없어지지 않는다. 식품을 통한 납의 주요노출 경로는 통조림 식품에 주로 존재하며 다른 식품에도 폭넓게 존재한다. 오염된 토양에서 재배된 농작물에도 높은 농도로 납이 존재할 수 있다. 따라서 식품에 의한 1일 섭취량은 100 μg 이하이며 때로는 500 μg 이상인 경우도 있다.위해성
납중독은 급성중독은 거의 없고 대부분이 만성중독이다. 식품을 통해 흡수된 납이 간으로 들어가 대부분은 담즙을 통해 대변으로 배설되지만 일부는 혈액을 통해 뼈 등의 조직에 침착한다. 납은 신체의 거의 모든 기관, 특히 중추 신경계에 가장 많은 영향을 미치며 심한 경우 사망에 이른다. 소량씩이라도 혈액, 신장, 골수, 간, 뇌 등과 같은 연조직 (軟組織)에 흡수·축적되며 혈액 속의 납은 뼈 속에 평생 동안 축적된다. 또한 혈액으로 유입된 납은 헤모글로빈 합성을 저해하여 빈혈을 유발하고, 고혈압이나 신장 기능 부전 등의 순환계 장해를 일으킨다. 특히 중추 신경계에 영향을 미쳐 반응시간 단축·기억력 감퇴 등과 같은 신경 장해, 과민반응, 뇌 손상, 정신장해 등을 일으킨다.오염실태
납은 독성이 강하므로, 국제적으로 납의 사용을 규제하려는 움직임이 활발한 중금속이다. 특히 미국의 경우 식품 캔에 납땜하는 것이 금지되어 있으며, 식품 캔 제조업체들은 자발적으로 캔 재질에 납이 함유되지 않은 것을 사용하고 있다. 가정에서 납 섭취를 줄이기 위해서는 식품을 개봉한 캔 또는 유약 처리가 완전하지 않는 도자기류에 음식을 조리하거나 담아 보관하지 말아야 한다. 어린이들이 더럽거나 페인트를 칠한 물건을 입에 넣지 않도록 주의해야 하며 집 안, 바닥과 창틀을 깨끗이 청소하고, 또한 고무젖꼭지, 장난감 및 천으로 만든 인형들은 정기적으로 씻어 주며 식사나 잠자기 전에 손을 씻는다. 칼슘은 뼈와 치아를 튼튼하게 할 뿐만 아니라 몸에 들어온 납의 흡수를 차단하여 납중독을 막아주는 효과가 있는 것으로 밝혀져 있으므로 칼슘 함량이 높은 시금치나 유제품들을 많이 섭취하는 것도 납중독을 막는 좋은 방법이며 또한 저지방 식품을 먹는 것도 납의 흡수를 낮추는 데 도움을 준다.국내외 관리현황
| 중금속명 | 기준치 (mg/kg) | 대상식품(수산물) |
|---|---|---|
| [식품의약품안전처, 2020] | ||
| 납 | 0.5 이하 | 어류 |
| 2.0 이하 (다만, 오징어는 1.0 이하, 내장을 포함한 낙지는 2.0 이하) |
연체류 | |
| 0.5 이하 (다만, 내장을 포함한 꽃게류는 2.0 이하) |
갑각류 | |
| 0.5 이하 [미역(미역귀 포함)에 한한다.] |
해조류 | |
| 0.5 이하 | 냉동식용 어류머리 | |
| 0.5 이하 (다만, 두족류는 2.0 이하) |
냉동식용 어류내장 | |
카드뮴
카드뮴은 자연계에 존재하는 금속물질의 하나로 지각 (crust) 중의 카드뮴 농도는 평균 0.1 mg/kg 수준으로 존재하며, 보통 오염되지 않는 수질의 경우 1 μg/kg이하 이다. 카드뮴은 푸른빛을 띤 은백색의 광택이 많이 나는 금속이다. 순수한 카드뮴은 부드러운 은색 금속이지만, 자연 환경에서는 산소, 염소, 황과 같은 원소와 결합하여 여러 가지 화합물 형태로 존재한다. 이런 화합물들은 대부분 안정한 고체이지만, 가끔 산화카드뮴은 작은 입자로서 공기 중에 존재하기도 한다. 산업에서 사용되고 있는 대부분의 카드뮴은 아연, 납, 구리 광석을 녹일 때 부산물로 얻어진 것이다. 주로 배터리, 색소, 금속 도금, 플라스틱 등에도 많이 사용된다. 진노란색 카드뮴 증기나 먼지를 흡입하면 카드뮴에 중독되고, 반감기가 대단히 길 뿐 만 아니라 축적된 카드뮴은 배설 또는 대사되기 어려운 금속이기 때문에 더욱 문제시 되고 있다.
발생원
대부분의 모든 자연식품에서 카드뮴이 검출되지만, 식물성 식품에서는 곡물류에 많이 분포하고 있으며, 동물성 식품에서는 어패류 및 해조류에 많이 분포되어 있다. 일반적으로 우리나라와 일본 등 쌀을 주식으로 하는 아시아 국가들에서는 쌀의 섭취를 통한 카드뮴의 노출이 비직업적 노출의 주요원인으로 알려져 있다.위해성
카드뮴은 대부분 호흡기를 통해 흡수되는데, 갓 생성된 카드뮴 증기는 흡입될 경우 폐에 침착이 잘된다. 또한 카드뮴은 위장을 통해서도 5% 정도가 흡수되며 카드뮴으로 처리한 용기에 담긴 산성 음식이나 음료수를 섭취하여도 카드뮴에 중독될 수 있다. 체내에 들어온 카드뮴은 간으로 이동되어 주로 간과 신장에 저장된다. 카드뮴 중독의 초기 증상은 뚜렷한 것이 없기 때문에 위험을 느끼지 못하며, 간혹 오한· 두통· 구토· 설사 등이 나타나 몸살감기 등으로 오인할 수 있다. 카드뮴에 장기간 노출되었을 때, 가장 먼저 이상이 나타나는 기관은 신장으로 소변에서 뇨단백이 검출된다. 심한 만성 중독의 경우, 드물지만 뼈에 병변 (골연화증, 골다공증, 특발성 골절)이 나타날 수 있다. 카드뮴 중독의 가장 대표적인 예는 이타이이타이병이 있다.오염실태
납은 독성이 강하므로, 국제적으로 납의 사용을 규제하려는 움직임이 활발한 중금속이다. 특히 미국의 경우 식품 캔에 납땜하는 것이 금지되어 있으며, 식품 캔 제조업체들은 자발적으로 캔 재질에 납이 함유되지 않은 것을 사용하고 있다. 가정에서 납 섭취를 줄이기 위해서는 식품을 개봉한 캔 또는 유약 처리가 완전하지 않는 도자기류에 음식을 조리하거나 담아 보관하지 말아야 한다. 어린이들이 더럽거나 페인트를 칠한 물건을 입에 넣지 않도록 주의해야 하며 집 안, 바닥과 창틀을 깨끗이 청소하고, 또한 고무젖꼭지, 장난감 및 천으로 만든 인형들은 정기적으로 씻어 주며 식사나 잠자기 전에 손을 씻는다. 칼슘은 뼈와 치아를 튼튼하게 할 뿐만 아니라 몸에 들어온 납의 흡수를 차단하여 납중독을 막아주는 효과가 있는 것으로 밝혀져 있으므로 칼슘 함량이 높은 시금치나 유제품들을 많이 섭취하는 것도 납중독을 막는 좋은 방법이며 또한 저지방 식품을 먹는 것도 납의 흡수를 낮추는 데 도움을 준다.국내외 관리현황
| 중금속명 | 기준치 (mg/kg) | 대상식품(수산물) |
|---|---|---|
| [식품의약품안전처, 2020] | ||
| 카드뮴 | 0.1 이하(민물 및 회유 어류에 한한다) 0.2 이하(해양어류에 한한다) |
어류 |
| 2.0 이하(다만, 내장을 포함한 낙지는 3.0 이하) | 연체류 | |
| 1.0 이하(다만, 내장을 포함한 꽃게류는 5.0 이하) | 갑각류 | |
| 0.3 이하[김(조미김 포함) 또는 미역(미역귀 포함)에 한한다.] | 해조류 | |
| - | 냉동식용 어류머리 | |
| 3.0 이하(다만, 어류의 알은 1.0 이하, 두족류는 2.0 이하) | 냉동식용 어류내장 | |
수은
수은 (Hg)은 상온에서 액체상태로 존재하는 유일한 금속으로 다양한 자연적 또는 인공적인 발생원으로부터 무기 수은 화합물의 형태로 환경 중에 방출되게 된다. 이러한 무기 수은은 토양과 퇴적물 내 미생물의 활동으로 유기형태인 메틸수은으로 전환된다. 환경으로 배출된 유기수은은 생태계의 먹이연쇄과정을 거치면서 고등한 생물체에 농축되기 때문에 수생 먹이사슬의 가장 높은 위치에 있는 장수 포식성 어종의 경우 많은 양의 메틸수은이 축적되게 된다. 수은은 인체에 누적될 경우 신경계통 등에 치명적인 피해를 주는 중금속의 하나로 온도계, 압력계, 형광등, 아말감에 사용되며, 각종 수은화합물은 살균제, 살충제, 건전지, 곰팡이 제거제, 방청 페인트, 안료 등의 재료로 쓰인다. 또 펄프나 종이, 아세트산, 염소, 가성소다의 제조공정에 이용되기도 한다. 수은에는 무기 수은과 유기 수은이 있다. 수은의 대부분은 무기 수은으로 온도계와 기압계에 많이 사용된다. 생물 농축의 주범인 수은은 유기 수은의 한 종류인 메틸수은이다. 유기수은은 지방용해도가 높아서 소화관에서의 흡수가 빠르고 혈액수액관문과 태반관문을 쉽게 통과할 수 있으며, 지방성분이 많은 중추신경계통에 독성을 나타낼 수 있다.
발생원
수은은 우리의 주변 환경에서 오랜 기간 잔류하는 동안 유기 수은이 무기 수은으로 되기도 하고, 반대로 무기 수은이 흙과 물 속에서 미생물과 바이러스의 생화학적 작용에 의해 천천히 유기 수은으로 바뀌기도 한다. 수은은 인체에 누적될 경우 신경계통에 치명적인 피해를 주는 중금속으로 온도계, 형광등, 살균제, 살충제, 페인트, 안료 등의 재료로 쓰인다. 이러한 수은은 강물이나 해저바닥의 혐기성 상태에서 미생물에 의하여 methylation되거나 공장 내에서 플라스틱 제품생산의 촉매로 사용된 수은이 플랑크톤, 어패류에 섭취되고 생태계의 먹이연쇄과정을 거치면서 고등한 생물체에 농축되기 때문에 수생 먹이사슬의 가장 높은 위치에 있는 장수 포식성 어종의 경우 많은 양의 메틸수은이 축적되게 되며 이로 인해 인간에 피해를 줄 수 있다.위해성
수은은 다른 중금속과 마찬가지로 한 번 몸 안에 들어오면 빠져나가지 않고 계속 누적되며 이것이 몸 안에 축적되어 총 수은량이 30 mg/kg 이상이 되면 수은 중독 현상을 일으키게 된다. 수은은 상온에서 천천히 증발하여 호흡기를 통하여 흡수되며 드물지만 소화기를 통하여 수은과 그 화합물이 흡수될 수도 있다. 이렇게 호흡기와 소화기로 흡수된 수은은 80% 정도가 신장 및 간에 축적되어 소뇌의 기능을 마비시킨다. 수은의 축적에 의한 중독은 만성 신경계의 질환으로 인해 운동장애, 언어장애, 난청, 심하면 사지가 마비되어 죽음에까지 이르기도 한다. 뿐만 아니라 산모가 이 병에 걸리게 되면 태아가 이와 같은 신경계 질환으로 인해 지체부자유자로 태어나기도 한다. 수은으로 인한 사람의 중독량은 5 mg/70 kg이며, 150~300 mg/70 kg 이상에 노출되면 사망하고, 독성도 무기수은에 비해 메틸수은 같은 유기수은이 훨씬 강하다. 식품에서의 무기 수은화합물 흡수는 섭취량의 7~8 %에 비하여 메틸수은은 위장에서 완전 흡수된다. 또한 물에서의 무기수은 화합물의 흡수는 15 %이하이고, 경구섭취하여도 무기수은은 체내에 흡수되지 않아 독성이 매우 약하여 그대로 대변으로 배설되는 반면 메틸수은은 거의 완전하게 흡수되며, 무기수은 화합물의 경우는 신장에서 축적될 수 있다.오염실태
메틸수은의 중독성이 최초로 보고된 것은 1950년대 일본 구마모토현 미나마타만에서 대규모 수은중독이 발생하여 미나마타병을 일으킨 사건이다. 이 사건은 메틸수은에 의한 중독증의 예로 1956년 일본의 미나마타현의 아세트알데히드 초산공장이 배출한 폐수로 인하여 발생하였다.국내외 관리현황
| 중금속명 | 기준치 (mg/kg) | 대상식품(수산물) |
|---|---|---|
| [식품의약품안전처, 2020] | ||
| 수은 | 0.5 이하 [아래(*) 어류는 제외한다] |
어류 |
| 0.5 이하 | 연체류 | |
| - | 갑각류 | |
| - | 해조류 | |
| 0.5 이하 [아래(*) 어류는 제외한다] |
냉동식용 어류머리 | |
| 0.5 이하 [아래(*) 어류는 제외한다] |
냉동식용 어류내장 | |
| 메틸수은 | 1.0 이하 [아래(*) 어류에 한한다] |
어류 |
| - | 연체류 | |
| - | 갑각류 | |
| - | 해조류 | |
| 1.0 이하 [아래(*) 어류에 한한다] |
냉동식용 어류머리 | |
| 1.0 이하 [아래(*) 어류에 한한다] |
냉동식용 어류내장 | |
| * 메틸수은 규격 적용 대상 해양어류 : 쏨뱅이류(적어포함, 연안성 제외), 금눈돔, 칠성상어, 얼룩상어, 악상어, 청상아리, 곱상어, 귀상어, 은상어, 청새리상어, 흑기흉상어, 다금바리, 체장메기(홍메기), 블랙오레오도리(Allocyttus niger), 남방달고기(Pseudocyttus maculatus), 오렌지라피(Hoplostethus tlanticus), 붉평치, 먹장어(연안성 제외), 흑점샛돔(은샛돔), 이빨고기, 은민대구(뉴질랜드계군에 한함), 은대구, 다랑어류, 돛새치, 청새치, 녹새치, 백새치, 황새치, 몽치다래, 물치다래 | ||
비소
비소는 다양한 형태의 화합물로 환경 중에 널리 분포하는 금속물질로서 강한 독성을 가지고 있는 주요 환경오염물질이다. 비소 화합물은 산소(O), 염소(Cl), 및 황(S)과 결합한 무기 비소 화합물과 탄소(C)와 수소(H)와 결합한 유기 비소 화합물로 나뉘며 비소의 인체에 대한 위해성은 이온의 상태나 화합물의 형태에 따라 다른 것으로 알려져 있다. 지각(crust) 중의 비소 농도는 평균 1.8 mg/kg정도이다. 우리나라 논, 토양 중 자연 함유량을 조사한 결과 평균 0.56 mg/kg(가용성), 현미 중 함유량은 0.088 mg/kg으로 나타났으며(1988), 농작물에 영향을 주는 농도는 10∼20 mg/kg으로 알려져 있다. 비소는 지구상의 어떤 시료를 취하여 분석하여도 어디서나 검출된다. 토양에서는 3∼10 mg/kg(국소적으로는 자연 함유량으로 500 mg/kg가 검출되었다는 보고도 있음)이 검출된다. 해수에서는 3∼10 μg/kg, 빗물은 0∼14 μg/kg, 대기에서는 0∼수백분의 1㎍/㎥ (주로 분진에 포함)이 검출된다. 광산, 제련소, 아비산, 비산염 등의 제조공장, 사용공정(반도체제조, 유리공업 등), 광산, 제련소, 공장 등에서 나오는 폐수, 광재, 분진 등의 비소뿐만 아니라 수목, 농작물에 사용된 살충제 중의 비소가 주변지역의 토양과 우물, 하천 등에 오염된다.
발생원
사람의 경우 비소에 노출되는 주요 경로는 호흡기(코)와 소화기계(입)이며 피부를 통한 노출은 매우 미미하다. 금속 제련업, 살충제 제조업, 목재 운반 및 가공업 등 비소화합물을 취급하는 사업장 근로자의 경우 비소의 주된 노출경로는 호흡기로서 주로 금속 또는 무기비소화합물이 주요 노출원이 된다. 그러나 비소에 특별히 폭로된 적이 없는 일반 주민들에 있어서 비소의 노출원은 비소에 오염된 물과 오염된 토양에서 재배된 농작물 및 어패류 등에 의해 구강을 통해서 주로 노출된다. 생체의 독성에 있어서 중요한 것은 무기비소화합물인데, 이는 자체의 독성과 함께 환경 중에서 비교적 이동이 자유롭기 때문에 식품이나 음용수에 오염되는 경우가 많기 때문이다. 산업적으로 가장 중요한 비소화합물은 arsenic trioxide(As2O3)이며 이는 구리나 납의 제련 과정에서 생산된다. 따라서 환경 중 비소의 오염은 (1) 산업폐기물의 처리, (2) 구리나 기타 금속의 제조, (3) 화석연료의 사용, (4)살충제, 제초제로의 이용 등을 통하여 이루어지며 인간에 노출은 주로 식품, 음용수 등을 통하여 만성적으로 노출되기 쉽다위해성
비소는 급성 중독 시 구토와 설사를 동반하거나 혈관호흡중추가 마비되기도 하고, 영양장애, 신경염, 흑피종 등이 유발된다. 비소화합물의 독성영향은 화합물의 화학적, 물리적 성질에 따라 좌우되며 특히 삼산화비소(As203)의 인체 중독량은 5~50 mg/70kg, 치사량은 100~300 mg/70kg이다. 비소가 피부에 닿으면 피부가 헐거나 염증이 생기며 눈에 들어가면 눈이 아프고 결막염과 같은 염증이 일어난다. 비소가 든 물질을 먹었을 경우 급성중독 증상으로는 식도가 따갑고 화끈거리고 침을 삼킬 수 없고 위와 배가 심하게 아프며 토하거나 설사를 하게 된다. 특히 몸속의 물이 다 빠지게 되어 입이 마르고 혈관이 마비되어 피부가 차가워지며 혈압과 맥박수가 내려간다. 심하면 심장장애 등의 쇼크증상이 나타나 사망하게 된다. 살충, 살균제에 이용되고 있는 비산, 아비산염은 만성중독의 원인이 된다. 또한 비소화합물을 장기간 취급하면 피부가 흑변 또는 각화하며 신경이나 근육의 섬유에 이상을 주는 수가 있다. 만성적으로 중독이 되었을 경우에 처음에는 식욕이 떨어지고 힘이 없어지며 설사, 변비, 구역질이 나타나다가 눈꺼풀이 붓거나 눈에 염증이 생기고 목구멍이 아프며 때로는 콧속에 구멍이 뚫린다. 비소는 동, 납, 철 등의 많은 황화광물 속에 함유되어 있기 때문에 제련공장 등에서 작업 중에 비소가 들어있는 먼지나 증기 등을 마시게 되면 만성중독이 발생할 가능성이 있다.오염실태
일반 식품에는 0.5 mg/kg 정도로 존재하나 해산물의 함량이 높아 오징어나 새우에는 10 mg/kg 이상으로 존재하기도 한다. 다시마 등에서 50 mg/kg 이상 검출된 예도 있다.국내외 관리현황
수산물 중에서는 잔류허용기준치가 설정되어 있지 않으나 해조류(톳, 모자반)가 사용된 가공식품에는 무기비소 기준치가 설정되어 있다.| 중금속명 | 기준치 (mg/kg) | 대상식품(가공식품) |
|---|---|---|
| [식품의약품안전처, 2020] | ||
| 무기비소 | 0.1 이하(크릴유에 한한다) | 식물성유지류, 어유, 기타동물성유지, 혼합식용유, 향미유, 가공유지, 쇼트닝, 마가린 |
| 0.1 이하*(현미, 미강, 쌀눈, 톳 또는 모자반을 사용한 식품에 한함) | 영아용 조제유, 성장기용 조제유, 영아용 조제식, 성장기용 조제식, 영·유아용 곡류조제식, 기타 영·유아식, 영·유아용 특수조제식품[시행일 2020.1.1.] | |
| 0.1 이하*(현미, 미강, 쌀눈, 톳 또는 모자반을 사용한 식품에 한함) | 특수의료용도등식품(영·유아용 특수조제식품 제외), 과자, 시리얼류, 면류 | |
| 1 이하*(현미, 미강, 쌀눈, 톳 또는 모자반을 사용한 식품에 한함) | 기타식품** | |
| * 총비소 시험결과 무기비소 기준 초과 검출 시 무기비소로 시험하여 기준 적용 ** 기타식품은 영아용 조제유, 성장기용 조제유, 영아용 조제식, 성장기용 조제식, 영·유아용 곡류조제식, 기타 영·유아식, 특수의료용도 등 식품, 과자, 시리얼류, 면류를 제외한 모든 식품을 말한다. |
||
마비성패류독소
개요
- 마비성패류독(Paralytic shellfish poison, PSP)에 의한 중독은 와편모조류의 일종인 Alexandrium spp., Pyrodinium spp., Gymnodinium catenatum 등의 해양 식물성 유독 플랑크톤이 생산하는 독소로 이를 패류가 축적하고 그 패류를 섭취함으로서 일어나는 식중독이다. 이 독에 중독되었을 때 마비 증세를 나타내어 마비성 패류독이라 한다. 패독 중 가장 흔하고 무서운 독소이다.
- 마비성패류독의 중독경로는 독을 생성하는 플랑크톤을 섭취하는 1차 포식자로 이매패류, 갑각류, 원색동물, 연체동물, 절족동물 등이 있고, 고차 포식자로는 육식성 고둥, 혹은 어류, 조류가 있으며, 최종적으로 사람이 이들을 섭취하여 중독된다. 그러나 일본이나 미국의 경우 대부분의 식중독은 마비성패류독에 의하여 독화된 이매패류의 섭취에 의해 일어나며 우리나라도 홍합에 의한 식중독 사고가 보고된 바 있다.
- 홍합, 백합, 굴, 바지락, 피조개, 가리비 등 이매패류와 멍게, 미더덕 등의 피낭류에서 주로 검출된다.
물질정보
구조식
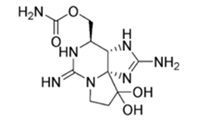
분석법
마우스시험법독성정보
식중독 증상
| 증상 | 정도 | ||
|---|---|---|---|
| 입술 주위가 따끔거리고 감각이 없어짐 위의 증상이 얼굴과 목으로 전이 손끝과 발끝 따끔거림 두통, 메스꺼움, 구토 |
경증 | 중증 | 극심한 증상 |
| 따끔거림/무감각 증상이 팔과 다리로 전이 현기증과 어눌한 발성 가벼운 호흡곤란 |
|||
| 마비증상이 온 몸으로 확산, 보행장애 심한 호흡곤란 및 질식 |
|||
발생사례
- 우리나라에서 공식적으로 알려진 중독사고는 6건으로 환자수는 사망자 5명을 포함한 46명이다. 1984년 5월 전남 목포에서 일가족 6명 중독, 1명 사망한 바 있고, 1986년 3월 부산 구평동에서 폐선 밑바닥에 붙어 있는 홍합을 먹고 25명이 중독되어 2명이 사망한 바 있으며, 1996년 5월에는 거제도 외포리에서 방파제에 붙어 있는 홍합을 끓여 먹고 2명이 사망하였다.
- 미국에서는 1930년부터 1954년 사이에 캘리포니아주에서만 373명이 중독되어 30명이 사망하였고, 일본에서도 1948년부터 1979년 사이에 93명이 중독되어 3명이 사망한 바 있다.
독성정보
규격기준 및 규제동향| 국가 | 식품 | 기준 |
|---|---|---|
| 한국 | 패류, 피낭류(멍게, 미더덕, 오만둥이 등) | 0.8 mg/kg 이하 |
| 미국 | 이매패류(가식부) | 80 μg/100g |
| 일본 | 패류 (가식부) | 4 MU/g |
| EU | 이매패류 (가식부) | 800 ug/kg |
| 호주 | 패류 (가식부) | 0.8 mg/kg |
참고자료
- 농식품 유해물질 편람. 농림수산식품부. 2009.
- 한국 연안의 진주담치 중 마비성패류독소. 2006.
- 수산식품안전의 이해. 부경대학교 출판부. 2010.
기억상실성패류독
개요
- 기억상실성패류독(amnesic shellfish poison, ASP)은 이매패류, 게(dungenes crab, Cancer magister), 바다가재 및 어류 등이 특정한 지역에서 발생하는 유독 규조류, Pseudonitzschia spp.를 직접 섭취하거나 또는 독성분이 축적된 생물을 섭취하여 독화되는 자연독의 하나이다.
- 독성분이 다량 축적된 이러한 수산물을 사람이 섭취하면 중독되며, 뿐만 아니라 멸치, 고등어 등 어류에 축적된 독성분은 펠리컨이나 바다사자 등 다른 동물에도 악영향을 미친다.
- 1987년 캐나다에서 이 식중독이 처음 발생하였을 때 나타난 증상이 다른 식중독과는 달리 특이하게 기억을 못하는 증상이 있어 기억상실성패류독이라고 부르고 있다.
물질정보
구조식
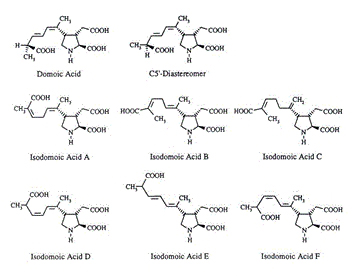
분석법
HPLC법, 질량분석법(LC-MS/MS)식중독증상
- 기억상실성패류독에 독화된 식품을 섭취 후 24시간 내에 구토, 설사, 복통 등 장관계 질환이 먼저 나타나고, 48시간 이내에 착란, 단기기억 상실(건망증과 유사함), 방향감각 상실 등과 같은 신경계 이상이 나타났다.
발생사례
- 우리나라에서는 기억상실성패류독에 의한 공식적인 식중독 사례는 보고되어 있지 않다.
- 1987년 캐나다에서 107명이 중독되어 3명이 사망한 사례가 최초의 기억상실성패류독 중독사건으로 보고되었고, 1990년대 초에 미국 서부에서도 기억상실성패류독에 의한 식중독 사고가 발생한 바 있다.
식품의 기준
| 국가 | 식품 | 기준 |
|---|---|---|
| 미국 | 이매패류(가식부) | 2 mg/100g |
| EU | 이매패류 (가식부) | 20 mg/kg |
| 호주 | 패류(가식부) | 20 mg/kg |
참고자료
- 농식품 유해물질 편람. 농림수산식품부. 2009.
- 수산식품안전의 이해. 부경대학교 출판부. 2010.
설사성패류독소
개요
- 설사성패류독(Diarrhetic shellfish poison, DSP)은 식물성 플랑크톤인 Dinophysis spp. 및 Prorocentrum spp. 등이 생성하는 독소로 이를 이매패류가 축적하고, 그 이매패류를 섭취함으로서 일어나는 식중독으로 1976년 일본의 미야기(宮城)현에서 홍합을 먹고 설사를 주 증상으로 하는 패류독 중독이 발생하였으며 주된 증상의 특징에서 설사성패류독으로 명명되었다.
- 설사성패류독은 마비성패류도과 달리 중독증상이 비교적 가벼운 소화기계 장해가 주 증상이며, 설사성패류독은 주로 중장선에 축적된다.
- 홍합, 굴, 모시조개, 바지락, 가리비 등 이매패류에 주로 존재하며, 이매패류의 독화 정도는 계절, 지역에 따라 달라지며 동일 지역에서도 수심에 따라 차이가 있다
물질정보
구조식
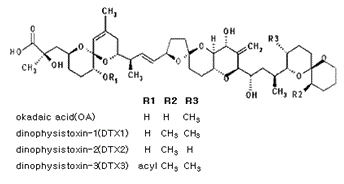
분석법
질량분석법(LC-MS/MS)식중독증상
설사성패류독의 중독증상은 소화기계 장해가 주 증상으로, 비교적 경증이다. 가장 발현률이 높은 증상은 설사(100%)이고 메스꺼움(80%), 복통과 구토(60%) 등이며, 발열은 거의 없다. 원인식품 섭취로부터 발증까지를 나타내는 잠복기는 비교적 짧아 70%의 환자가 섭취 후 4시간 이내에 발증하며, 심하면 30분 내에 발증하는 경우도 있다. 설사는 수양변이며 특별한 치료를 하지 않아도 거의 3일 이내에 희복하며, 사망 예는 없다.발생사례
- 우리나라에서는 기억상실성패류독에 의한 공식적인 식중독 사례는 보고되어 있지 않다.
- 일본에서는 1976년부터 1983년 사이에 1,300명 이상의 환자가 발생한 바 있고, 1981년에는 스페인에서 5,000명, 1983년에는 프랑스에서 3,394명의 중독환자가 발생한 바 있다.
식품의 기준
| 국가 | 식품 | 기준 |
|---|---|---|
| 한국 | 이매패류 | 0.16 mg/kg 이하 |
| 미국 | 이매패류 (가식부) | 0.16 mg/kg |
| 일본 | 패류 (가식부) | 0.05 MU/g |
| EU | 이매패류 (가식부) | 160 ug/kg |
| 호주 | 패류(가식부) | 0.2 mg/kg |
참고자료
- 농식품 유해물질 편람. 농림수산식품부. 2009.
- 농식품 중 위해요소의 Risk profile. 농촌진흥청 국립농업과학원. 2012.
- 수산식품안전의 이해. 부경대학교 출판부. 2010.
복어독
개요
- 복어에는 독이 있고 잘못하면 목숨을 잃는다는 것은 옛날부터 잘 알려져 왔으며, 약 2,200년 전에 중국에서 쓰여진 진의 시황제 시대의 “山海經”에도 복어가 사람을 죽인다고 기록되어 있다(野口, 1996).
- 중독 초기증상으로 입술이나 혀끝이 마비되며, 이 마비증세는 얼굴과 손가락에서 사지로 확산되어 결국에는 운동능력을 상실하여 보행이 곤란하게 된다.
- 전 세계적으로 우리나라와 일본을 제외하면 공식적으로 복어를 먹을 수 있는 나라는 드물다. 중국은 이전에는 복어를 많이 먹었다고 하나 최근에는 법으로 유통과 판매를 금지하고 있다.
물질정보
구조식
복어독을 보유하는 생물에서 독성분은 테트로도톡신(Tetrodotoxin;TTX) 단일 성분으로 존재하지 않고 몇 종류의 유도체가 복합적으로 구성되어 있다
분석법
마우스시험법, 질량분석법(LC-MS/MS)식중독증상
- 복어독은 전형적인 신경독으로 섭취한 후 증상이 나타날 때까지의 잠복기는 약 20~30분에서 6시간 정도로 증상이 심할수록 잠복기가 짧다.
- 일본에서는 1976년부터 1983년 사이에 1,300명 이상의 환자가 발생한 바 있고, 1981년에는 스페인에서 5,000명, 1983년에는 프랑스에서 3,394명의 중독환자가 발생한 바 있다.
- 증상이 더 심해지면 혀나 목이 마비되어 음식을 삼키는 것이나 언어 및 발성이 곤란해지며, 결국에는 전신의 반사기능이 소실되고 혈압저하와 호흡마비로 사망한다.
발생사례
우리나라에서 1971~1986년 사이에 발생한 복어독 중독 사건은 총 44건으로 147명이 중독되어 그 중 51명이 사망하였으며, 1991~2002년 사이에는 총 32건이 발생하여 111명이 중독되었고 그 중 30명이 사망하였다.식품의 기준
(1) 육질 : 10 MU/g 이하 / (2) 껍질 : 10 MU/g 이하 / (3) 식용가능한 복어의 종류| 연번 | 종류 | 학명 |
|---|---|---|
| 1 | 복섬 | Fugu niphobles, Takifugu niphobles |
| 2 | 흰점복 | Fugu poecilonotus, Takifugu poecilonotus |
| 3 | 졸복 | Fugu pardalis, Takifugu pardalis |
| 4 | 매리복 | Fugu vermicularis vermicularis, Takifugu vermicuLaris snyderi |
| 5 | 검복 | Fugu vermicularis porphyreus, Takifugu porphyreus |
| 6 | 황복 | Fugu ocellatus obscurus, Takifugu obscurus |
| 7 | 눈불개복 | Fugu chrysops, Takifugu chrysops |
| 8 | 자주복 | Fugu rubripes, Takifugu rubripes |
| 9 | 검자주복 | Fugu rubripes chinensis, Takifugu chinensis |
| 10 | 까치복 | Fugu xanthopterus, Takifugu xanthopterus |
| 11 | 금밀복 | Lagocephalus inermis |
| 12 | 흰밀복 | Lagocephalus wheeleri |
| 13 | 검은밀복 | Lagocephalus gloveri |
| 14 | 불룩복 | Sphoeroides pachygaster, Liosaccus pachygaster |
| 15 | 삼채복 | Fugu flavidus, Takifugu flavidus |
| 16 | 강담복 | ChiLomycterus affinis |
| 17 | 가시복 | Diodon holocanthus |
| 18 | 브리커가시복 | Diodon liturosus |
| 19 | 쥐복 | Diodon hystrix |
| 20 | 노란거북복 | Ostracion cubicus |
| 21 | 까칠복 | Fugu stictonotus, Takifugu stictonotus |
참고자료
- 농식품 유해물질 편람. 농림수산식품부. 2009.
- 농식품안전정보서비스 리스크프로파일. 농림수산식품교육문화정보원
- 수산식품안전의 이해. 부경대학교 출판부. 2010.
- 농식품 중 위해요소의 Risk profile. 농촌진흥청 국립농업과학원. 2012.
테트라민
개요
- 테트라민(Tetramine) 식중독은 해양고둥류인 관절매물고둥(Neptunea arthritica), 조각매물고둥(N. intersculpta), 갈색띠매물고둥(N. arthritica cumingii) 등을 섭취한 후 배멀미감을 동반하는 식중독의 하나이다.
- 테트라민 중독은 우리나라뿐만 아니라 일본, 영구, 노르웨이, 캐나다 등 북반구의 여러나라에서 보고되어 있다.
물질정보
구조식
복어독을 보유하는 생물에서 독성분은 테트로도톡신(Tetrodotoxin;TTX) 단일 성분으로 존재하지 않고 몇 종류의 유도체가 복합적으로 구성되어 있다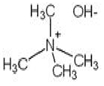
분석법
비색법, Ion chromathography, 질량분석법(LC-MS/MS)식중독증상
- 대부분의 환자에서 잠복기는 약 30분에서 1시간 정도이며, 주 증상은 안구통증, 두통, 현기증, 복통, 메스꺼움, 얼굴발열, 배멀미감 등 이다.
- 통상 2~3시간만에 회복되지만, 고령자에서는 수일 동안 증상이 나타나기도 한다.
중독예방
- 테트라민은 육식성 고둥류의 전 부위에 고루 퍼져 있는 것이 아니라 타액선에 집중되어 있으므로 조리시에 타액선을 제거하면 안전하다.
- 고둥류의 종류 및 크기에 따라 타액선의 색깔과 크기는 차이가 있지만, 색깔은 보통 우유빛 또는 황색을 띠고, 크기는 완두콩이며 육질부 내부에 들어있다.
- 테트라민은 열에 대단히 안정하여 삶거나 끓여도 독성이 없어지지 않으므로 고둥류를 조리하기 전에 타액선을 제거하는 것이 중요하다.
참고자료
- 수산식품안전의 이해. 부경대학교 출판부. 2010.
- 농식품 중 위해요소의 Risk profile. 농촌진흥청 국립농업과학원. 2012.
시구아테라
개요
- 시구아테라는 산호초와 해조류 표면에 부착하여 생육하는 플랑크톤(Gambierdiscus toxicus)이 생성하는 독소(시구아톡신, Ciguatoxin)에 독화된 어류를 사람이 섭취하면 발생하는 식중독이며, 이 독소는 내열성이 있어 조리 후에도 독성이 잔류한다.
- 시구아테라 발생경로는 산호초와 해조류 주변에서 생육하는 작은 물고기가 플랑크톤(Gambierdiscus toxicus)을 섭취하여 독화되고, 큰 물고기가 독화된 작은 물고기를 잡아먹음으로써 큰 물고기 체내에 시구아톡신이 농축되고, 이를 사람이 섭취하면 사람에게 식중독을 유발시킨다.
- 시구아테라(Ciguatera) 중독은 전 세계적으로 수산물 섭취와 관련한 식중독 중 세균성을 제외하면 가장 많은 환자가 발생하며 연간 10,000~50,000명이 중독되는 것으로 추정되고 있으나, 우리나라에서는 아직 시구아테라 식중독 사례가 보고되고 있지 않다.
- 시구아톡신을 생성하는 플랑크톤은 주로 남·북위 35도 이내의 열대 및 아열대 지방의 산호초가 발달한 해역에서 많이 발견되었지만, 기후변화 등의 영향으로 남북위 35°에서도 시구아톡신을 생성하는 플랑크톤이 발견되고 있다.
분석법
질량분석법(LC-MS/MS)식중독증상
- 시구아테라 중독 증상은 소화기계 증상 또는 신경계 증상 중 어느 것이나 먼저 나타났다. 소화기계 증상으로는 구토, 설사, 메스꺼움 및 복통과 관련된 위장 증상이 발병하며, 24시간~48시간 지속된다.
- 신경계 증상은 입술 및 손발의 따끔거림, 온도 인지 장애 등과 같은 신경 장애 증상이 드물게 나타나 몇 주에서 수개월까지 지속되기도 하고, 일부 사람에서는 특정 증상이 수년 동안 나타나기도 한다고 알려져 있다.
- 중독 증상이 매우 심한 경우에는 호흡 곤란 및 마비로 인한 저혈압 유발로 사망하는 경우도 있다.
관리현황
- 일본은 오키나와에서 중독사례가 보고되고 있어 시구아테라 중독 발생 사례가 있는 어종 중심으로 식용하지 않도록 지도하고 있다.
- 미국은 어류 중의 시구아톡신(태평양 및 카리브 형)에 대한 관리기준을 0.01 μg/kg 설정하여 관리하고 있으며, 또한 식중독 예방을 위해 시구아톡신 발생해역에서의 어류 포획 자제를 지도하고 있다.
- 유럽연합에서는 시구아톡신이 함유되어 있는 어류는 시장에 출하 시킬 수 없다.
참고자료
- 수산식품안전의 이해. 부경대학교 출판부. 2010.
신경성패류독소
개요
- 신경성패류독(neurotoxic shellfish poison, NSP)은 편모조류인 Karenia brevis이 생성하는 독소로 패류를 독화시켜 식중독을 유발한다는 것이 오래 전부터 알려져 있다.
- 신경성패류독은 두 가지의 중독경로가 있다. 패류를 섭취하여 발생하는 식중독과 Karenia brevis 플랑크톤은 파도 등 물리적 자극에 의해 쉽게 부셔져 비산한 것을 호흡을 통하여 흡입함으로써 호흡계 장해 증세가 나타나는 비말중독으로 나누어진다.
물질정보
구조식
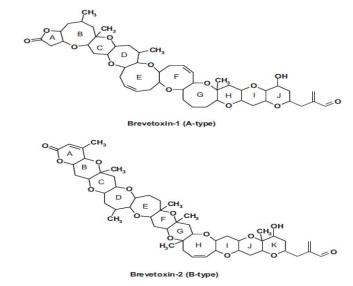
분석법
마우스시험법식중독증상
- 식중독 증상은 식후 약 30분에서 3시간 후부터 얼굴, 입술 및 사지의 착감각증, 메스꺼움, 설사, 현기증, 구토, 목의 따끔거림, 혈압저하 등의 증상이 1시간에서 72시간 지속된다.
- 비말중독은 결막 자극감, 콧물, 기침, 기관지 수축 등의 증세를 나타내며 비교적 빨리 회복된다.
발생사례
- 우리나라에서는 신경성패류독에 의한 공식적인 식중독 발생 사례가 보고 되어 있지 않다.
- 뉴질랜드에서는 1992년 12월에서 1993년 1월에 홍합을 섭취한 186명이 신경성패류독에 중독되었으며, 미국 플로리다에서도 신경성패류독에 의한 식중독 환자가 발생하고 있다.
식품의 기준
| 국가 | 식품 | 기준 |
|---|---|---|
| 미국 | 이매패류 (가식부) | 20 MU/100g |
| 호주 | 패류 (가식부) | 200 MU/kg |
참고자료
- 수산식품안전의 이해. 부경대학교 출판부. 2010.
 이 누리집은 대한민국 공식 전자정부 누리집입니다.
이 누리집은 대한민국 공식 전자정부 누리집입니다.


